БИОЛОГИЧЕСКИ ВАЖНЫЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ.
Оглавление
- 1 БИОЛОГИЧЕСКИ ВАЖНЫЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ.
- 1.1 ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ.
- 1.2 Вода и её роль в жизнедеятельности клетки.
- 1.3 НЕОРГАНИЧЕСКИЕ ВЕЩЕСТВА КЛЕТКИ И ИХ БИОЛОГИЧЕСКАЯ РОЛЬ.
- 1.4 ОРГАНИЧЕСКИЕ ВЕЩЕСТВА КЛЕТКИ.
- 1.5 ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №1 «Роль белков, углеводов и жиров в организме человека. Витамины.»
- 1.6 ЛАБОРАТОРНАЯ РАБОТА №1 «Определение витамина С в продуктах питания. Гидрофильно-гидрофобные свойства липидов.«
- 1.6.1 БИОЛОГИЧЕСКАЯ ЦЕННОСТЬ ВИТАМИНА С.
- 1.6.2 СУТОЧНАЯ ПОТРЕБНОСТЬ В ВИТАМИНЕ С.
- 1.6.3 ВИТАМИННАЯ НЕДОСТАТОЧНОСТЬ – АВИТАМИНОЗ.
- 1.6.4 ГИПЕРВИТАМИНОЗ.
- 1.6.5 ПРОФИЛАКТИКА АВИТАМИНОЗА.
- 1.6.6 ИСТОЧНИКИ ВИТАМИНА С.
- 1.6.7 ПРАКТИЧЕСКАЯ ЧАСТЬ. Количественное определение содержания витамина С в продуктах питания йодометрическим методом
- 1.6.8 ПРАКТИЧЕСКАЯ РАБОТА: Изучение свойств липидов и жироподобных веществ: растворимость, эмульгирование, качественная реакция на прогоркшие жиры.
ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ.
Любой живой организм состоит из тех же химических элементов, что и предмет неживой природы. Химические элементы входят в состав молекул органических и неорганических веществ, формирующих состав тела организма. Химические элементы входят в состав клеток в виде ионов или компонентов молекул неорганических и органических веществ. Относительно простые химические соединения, которые встречаются как в живой, так и в неживой природе (в минералах, природных водах), называют неорганическими (минеральными) веществами (вода, минеральные соли). Многообразные соединения углерода, синтезируемые преимущественно живыми организмами, называют органичес-кими веществами (углеводы, липиды, белки, нуклеиновые кислоты, витамины и др.).В живых клетках обнаружено около 70 элементов. Однако соотношение различных элементов в объектах живой и неживой природы неодинаково.

В клетках живых организмов на долю углерода, кислорода, азота и водорода приходится почти 98% массы. Относительное содержание этих элементов значительно выше, чем в земной коре. Они являются основ-ными компонентами органических соединений. Их называют макро-элементами. Жизненно необходимыми являются ещё восемь элемен-тов, содержание которых в клетке исчисляется десятыми и сотыми до-лями процента и в сумме составляет менее 2%. Это магний, натрий, кальций, железо, калий, сера, фосфор, хлор. Сера и фосфор входят в сос-тав молекул биополимеров. Натрий, калий и хлор участвуют в образо-вании разности зарядов внешней и внутренней поверхностей мембраны клетки, обусловливающей такие важные процессы, как передача возбуждения по нерву или мышце. Железо является компонентом гемоглобина. Кальций и фосфор, накапливаясь в костной ткани, прида-ют прочность костям. Магний входит в состав хлорофилла и многих ферментов.
К группе микроэлементов относят цинк, медь, йод, фтор, марганец, кобальт, кремний и другие элементы, содержа-щиеся в клетке в малых количествах (суммарное содержание порядка 0,1%). Несмотря на низкое содержание в живых организмах, микроэлементы играют важную роль: они входят в состав различных ферментов, гормонов, витаминов и обусловливают тем самым нормальное развитие и функциони-рование структур клетки и организма в целом: медь является составной частью ряда ферментов, занятых в процессах тканевого дыхания; цинк — необходимый компонент почти ста ферментов, в частности ДНК- и РНК-полимераз; он содержится также в гормоне поджелудочной железы — инсулине; кобальт входит в состав витамина В12, регулирующего кроветворную функцию; йод является компонентом гор-мона щитовидной железы — тироксина. При недостатке этих элементов в почве, в воде и в пищевых продуктах снижается их содержание и в организме. При этом развиваются различные патологические состояния (сахарный диабет, эндемический зоб, злокачественная анемия и др.).
Вода и её роль в жизнедеятельности клетки.
Обязательным условием жизнедеятельности клетки является наличие воды. Вода — одно из самых распространенных веществ на Земле и преобладающий компонент всех живых организмов. Среднее содержание воды в клетках большинства организмов составляет около 70% (в клетках медузы — 96%). У человека содержание воды в клетках костной ткани составляет 20%, жировой ткани — 40%, мышечной ткани — 70%, в клетках головного мозга — до 85%, а в клетках развивающегося зародыша — около 90%. Количество воды в различных органах и тканях варьирует и зависит от уровня их обменных процессов. Вода в клетке находится в двух формах: свободной и связанной. Свободная вода составляет 95% всей воды клетки; на долю связанной воды, входящей в состав фибриллярных структур и соединенной с некоторыми белками, приходится около 5%.

Роль воды в клетке определяется ее химическими и физическими свойствами. Вода обладает рядом свойств, имеющих исключительно важное значение для живых организмов. Уникальные свойства воды определяются структурой ее мо-лекул. Молекула воды является диполем. Атом кислорода в ней ковалентно связан с двумя атомами водорода. Положи-тельные заряды сосредоточены у атома водорода, так как кислород электроотрицательнее водорода. Молекулы воды способны образовывать между собой водородные связи. По прочности водородная связь примерно в 20 раз слабее ковалентной, поэтому она легко разрывается, например, при испарении воды.
Малые размеры молекул воды, их полярность и способность соединяться между собой водородными связями обеспе-чивают хорошее растворение в воде многих минеральных и органических веществ, газов и др. Вещества, хорошо растворимые в воде, называют гидрофильными. К ним относят многие кристаллические соли, ряд органических веществ — спирты, сахара, некоторые белки ( альбумины, гистоны). Вещества, плохо или вовсе не растворимые в воде, называют гидрофобными. Они представлены жирами, нуклеино-выми кислотами, некоторыми белками (глобулинами, фибриллярными белками).
Вода обладает высокой удельной теплоемкостью и теплопроводностью. Высокая теплоемкость воды, т.е. способность поглощать теплоту при минимальном изменении собственной температуры, делает ее идеальной жидкостью для поддержания теплового равновесия клетки и организма. Так как на испарение воды расходуется много теплоты, то, испаряя воду, организмы могут защищать себя от перегрева (при потоотделении). Вода обладает высокой теплопроводностью, обеспечивая возможность равномерного распределения теплоты между тканями организма. В результате устраняется риск температурного повреждения клеток.

Вода является дисперсионной средой, играющей важную роль в коллоидной системе цитоплазмы. Она определяет структуру и функцио-нальную активность многих макромолекул, служит основной средой для протекания химических реакций и непосредственным участни-ком реакций синтеза и расщепления органических веществ. Вода обеспечивает транспорт веществ в клетке и организме (диффузию, кровообращение, восходящий и нисходящий ток растворов по телу растения и др.). Вода практически не сжимается, создавая тургорное давление и определяя объем и упругость клеток и тканей. Клетки могут использовать воду в качестве источника кислорода и водорода, выделяемых в световую фазу фотосинтеза.
НЕОРГАНИЧЕСКИЕ ВЕЩЕСТВА КЛЕТКИ И ИХ БИОЛОГИЧЕСКАЯ РОЛЬ.
Неорганические соединения клетки чаще всего находятся в виде солей, диссоциированных в растворе на ионы. Также соли встречаются в твердом состоянии (карбонаты и фосфаты кальция костной ткани, известковые или кремневые панцири губок, раковин моллюсков, многих водорослей). Неорганические ионы имеют большое значение для обеспе-чения процессов жизнедеятельности клетки. Наиболее важ-ными для клеток являются катионы К+, Na+, Мg2+, Са2+ и анионы HPO42-, Н2РO4—, Сl—, НСO3— минеральных солей. Соли натрия, калия, каль-ция и др. составляют около 0,9 — 1% плазмы крови. Концентрация различных солей в плазме относительно постоянна.
Состав минеральных солей и их концентрация определяют осмотическое давление внутри клеток. Плазматическая мембрана обладает избирательной проницаемостью. Она пропускает молекулы воды, но непроницаема для более крупных молекул растворенных в воде веществ. Процесс диффузии молекул воды через полупроницаемую мембрану в направлении большей концентрации растворенного в ней вещества называют осмосом. Осмотическое давление зависит от содержания в растворе солей, белков и др. Явление осмоса играет важную роль. Благодаря осмосу регули-руется поступление воды в клетки и межклеточные структуры. Упругость клеток (тургор), обеспечивающая эластич-ность тканей и сохранение определенной формы органов, обусловлена осмотическим давлением.

Растворы, имеющие одинаковое осмотическое давление, называют изотоническими. Для теплокровных животных и человека изотоническими растворами являются 0,9%-ный раствор NaCl и 4,5%-ный раствор глюкозы. Изотонические растворы, приближающиеся по составу, ве-личине рН, буферным и другим свойствам к плазме крови, называют физиологическими растворами. Такие растворы используются в качестве кровезаменителей. При помещении клеток в такой раствор они сохраняют свой размер и нормально функционируют. Лекарства, пред-назначенные для введения в кровь, растворяют в физиологическом растворе. Если же ввести в кровь слишком концентрированный раствор хлорида натрия (3 — 5— 10%-ный, гипертонический раствор), то вода из клеток будет выходить наружу, и они сожмутся. Гипотонические растворы содержат соли в меньшем количестве, чем плазма крови (менее 0,9% NaСl), поэтому при помещении в такие растворы эритроцитов вода устремляется внутрь клетки (эритроцита), клетка набухает, что приводит к её разрыву. Концентрация катионов и анионов в клетке и в окружающей ее среде различна. Внутри клетки концентрация ионов К+ и крупных органических ионов больше, а за пределами клеток, в околокле-точных жидкостях, всегда больше ионов Na+ и Сl—. Вследствие этого образу-ется разность зарядов внешней и внут-ренней поверхностей мембраны клетки, между ними возникает разность потенциалов, обусловливающая такие важные процессы, как передача возбуждения по нерву или мышце. Для нормального сокращения сердечной мышцы мле-копитающих необходимо определенное соотношение К+, Na+ и Са2+. При нарушении баланса этих ионов работа сердечной мышцы нару-шается. Снижение уровня Са2+ в крови вызывает судороги и смерть. Содержащиеся в организме ионы имеют важное значение для под-держания постоянства реакций среды в клетке (гомеостаза) и в окружающих ее растворах, т.е. являются компонентами буферных систем. Буферы поддерживают слабощелочную реакцию содержимого клеток на слабощелочном уровне. Наиболее значимыми буферными сис-темами млекопитающих являются фосфатная и бикарбонатная. Фосфатная буферная система состоит из НРО42- и Н2РO4— и поддерживает рН внутриклеточной жидкости в пределах 6,9 — 7,4. Главной буферной системой внеклеточной среды (плазмы крови) служит бикарбонат-ная система, состоящая из Н2СO3 и НСO3— и поддерживающая рН на уровне 7,4.
Соединения азота, фосфора, кальция и другие неорганические вещества служат источником строительного материала для синтеза орга-нических молекул (аминокислот, белков, нуклеиновых кислот и др.) и входят в состав ряда опорных структур клетки и организма. Соли кальция и фосфора входят в состав костной ткани животных. Некоторые неоргани-ческие ионы (ионы кальция и магния) являются актива-торами и компонентами многих ферментов, гормонов и вита-минов. При недостатке этих ионов нарушаются жизненно важные процессы в клетке. Соляная кислота входит в состав желудочного сока животных и человека, ускоряя процесс переваривания белков пищи. Остатки серной кислоты, при-соединяясь к нерастворимым в воде веществам, придают им растворимость, способствуя выведению из организма. Натриевые и калиевые соли азотистой и фосфорной кислот, кальциевая соль серной кислоты служат важными компо-нентами минерального питания растений, их вносят в почву в качестве удобрений.

- Качественный состав элементов, образующих неживую и живую материю, во многом сходен.
- Шесть основных элементов — Н, О, N. С, Р и S — называют биоэлементами, отмечая их вклад в образование органических молекул.
- Вода образует основу внутренней среды живых организмов.
- Катионы и анионы растворимых солей формируют буферные системы клетки, предотвращая резкие колебания рН внутренней среды.
Вопросы для самопроверки:
- Какие химические элементы входят в состав клетки? Приведите примеры биологической роли химических элементов.
- Что такое микроэлементы? Приведите примеры и охарактеризуйте их биологическое значение.
- Какие неорганические вещества входят в состав клетки?
- В чем заключается биологическая роль воды? Минеральных солей?
- Какие вещества обусловливают буферные свойства клетки?
- Каковы отличия вклада различных элементов в организацию живой и неживой природы?
- Объясните, как физико-химические свойства воды проявляются в обеспечении процессов жизнедеятельности клетки и целостного организма.
ОРГАНИЧЕСКИЕ ВЕЩЕСТВА КЛЕТКИ.
Химическими признаками живого служат органические соединения. Они составляют около 20 — 30% массы клетки живого организма и чрезвычайно многообразны. Наиболее важное значение в жизнедеятельности клеток имеют нуклеиновые кислоты (1 — 5%), белки (10 — 20%), липиды (5 — 10%) и углеводы (1 — 5%). Они являются структурными элементами клеток, а также их функциональными элементами, так как играют важную роль в процессах обмена веществ. Основу органических веществ составляют атомы углерода, способные вступать друг с другом в прочные ковалентные связи и образовывать разнообразные по форме каркасы органических молекул. В зависимости от молекулярной массы и структуры различают малые, низкомолекулярные органические молекулы — мономеры и более крупные, высоко-молекулярные макромолекулы — полимеры. Мономеры служат строительными блоками для полимеров. Полимеры представляют собой линейные или разветвленные цепи, содержащие большое число мономерных звеньев. Свойства биополимеров зависят от числа, состава и порядка расположения составляющих их мономеров. Возможность изменения состава и последовательности мономеров в структуре полимера лежит в основе образования значительного числа вариантов биологических макромолекул, обладающих различными свойст-вами. Этот принцип играет важную роль в понимании многообразия живых организмов.
Углеводы и их роль в жизнедеятельности клетки.
Содержание углеводов в животных клетках составляет 1 — 5%, а в клетках некоторых растений достигает 70%. Углеводы состоят из угле-рода, водорода и кислорода. Как следует из названия, углеводы представляют собой соединения углерода и воды. Существуют три основ-ных класса углеводов: моносахариды, олигосахариды и полисахариды, различающихеся числом мономерных звеньев.

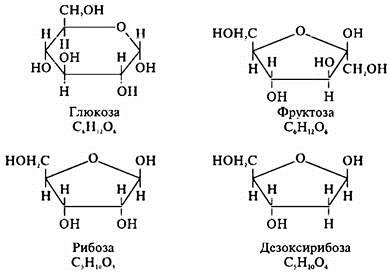
Моносахариды — бесцветные твердые кристаллические вещества, легко растворимые в воде, но нерастворимые в неполярных растворителях, имеющие сладкий вкус. В зависимости от числа атомов углерода различают: триозы, тетрозы, пентозы, гексозы и гептозы. Наиболее распро-странены в природе гексозы (глюкоза, фруктоза, галактоза) — основные источники энергии в клетках (при полном расщеплении 1 г глюкозы высвобождается 17,6 кДж энергии) и пентозы (рибоза, дезоксирибоза), входящие в состав нуклеотидов нуклеиновых кислот. В обмене веществ участвуют главным образом в форме фосфатов.

Два или несколько ковалентно связанных друг с другом с по-мощью гликозидной связи моносахарида образуют ди-, или олигосахариды. Дисахариды также широко распространены в природе: наиболее часто встречаются сахароза (сахар, получаемый из сахарного тростника или свеклы), состоящая из глюкозы и фруктозы; мальтоза (солодовый сахар), образованная двумя молекулами глю-козы; лактоза (молочный сахар), входящая в состав молока и состоящая из галактозы и глюкозы. Дисахариды близки по своим свойствам к моносахаридам, хорошо растворимы в воде и имеют сладкий вкус.
Полисахариды — это биополимеры, содержащие большое число моносахаридных остатков, связанных гликозидной связью, и обладающие высокой молекулярной массой. Они утрачивают сладкий вкус и способность растворяться в воде. В составе организмов имеется много полисахаридов: крахмал, используемые клетками растений и гликоген, используемый клетками животных для запасания энер-гии, а также целлюлоза и хитин, обеспечивающие прочность покровных структур растений, грибов и животных. В частности, в состав клеточной стенки клеток растений входит около 20 — 40% целлюлозы. Многие полисахариды животных образуют соединения с белками (гликопротеины) и липидами (гликолипиды). Гликолипиды участвуют в построении клеточных мембран. Гликопротеины (например, гепарин) регулируют свертывание крови, липидный обмен.

Некоторые углеводы способны образовывать комплексы с липидами и белками, формируя сложные углеводы типа гликолипидов и гликопротеинов. Большинство мембранных и секретируемых клеткой белков относится к гликопротеинам.
Функции углеводов многообразны.
- Они являются мощным и богатым источником энергии, необходимой клетке для осуществления различных форм активности. При окислении 1 г углеводов выделяется 17,6 кДж (для этой цели, как правило, используется глюкоза).
- Полисахариды — удобная форма накопления энергоемких моносахаридов (в виде крахмала у растений и гликогена у животных), а также незаменимый защитный и структурный компонент клеток и тканей животных, растений и микроорганизмов.
- Целлюлоза образует стенки растительных клеток, а сложный полисахарид хитин является главным структурным компонентом наружного скелета членистоногих.
- Небольшие олигосахариды, включающие 20 — 30 мономерных звеньев, входят в состав клеточных мембран и служат рецепторами, обеспечивая узнавание клеток друг другом и их взаимодействие.

- Наибольшее количество углеводов содержится в растительных клетках.
- Моносахариды являются основным источником энергии для большинства живых организмов.
- Углеводы входят в состав рецепторов клетки и поверхностных антигенов, выполняя информационно-коммуникативные функции.
- Полисахарид целлюлоза входит в состав клеточных стенок прокариот и растений.
- Хитин образует наружный скелет членистоногих и клеточные оболочки грибов.
Липиды и их роль в жизнедеятельности клетки.
Липиды — органические вещества, нерастворимые в воде, но хорошо растворимые в органических растворителях — эфире, хлороформе, бензоле. Они обнаружены во всех без исключения клетках и разделены на несколько классов, выполняющих специфические биологичес-кие функции. Количество липидов в разных клетках варьирует от 2— 3 до 50 — 90% в клетках семян растений и жировой ткани животных. Наиболее распространенными в составе живой природы являются нейтральные жиры, или триацилглицерины, воски, фосфолипиды, стиролы. По химической структуре жиры представляют собой соединения трехатомного спирта глицерина и высокомолекулярных жирных кислот. Воски — эфиры одноатомного спирта и жирных кислот. Фосфолипиды построены так же, как жиры, но отличаются от последних наличием остатка фосфорной кислоты. Сложные липиды представляют собой эфиры спирта, жирных кислот и других веществ (гликопро-теиды состоят из белков и липидов, гликолипиды — из углеводов и липидов). Значение липидов огромно:

• Жирные кислоты являются ценным источником энергии. При окислении 1 г ли-пидов высвобождается 38,9 кДж энергии и синтезируется в два раза большее количество АТФ, чем при расщеплении такого же количества глюкозы.
• Нейтральные жиры накапливаются клетками для последующего использования в качестве источника энергии или пластического материала. У позвоночных животных примерно половина энергии, потребляемой клетками в состоянии покоя, образуется за счет окисления жиров.
• Жиры используются также в качестве источника воды (при окислении 100 г жира образуется более 100 мл воды). Это особенно ценно для арктических и пустынных животных, обитающих в условиях дефицита свободной воды.
• У многих млекопитающих под кожей откладывается толстый слой подкожного жира, который благодаря низкой теплопроводности защищает организм от переохлаждения.
• Фосфолипиды и сфингомиелины являются основой клеточных мембран.
• Жиры участвуют в растворении гидрофобных органических соединений, например, витаминов А, D, Е, необходимых для нормального протекания биохимических превращений в организме.
• Стероиды составляют группу липидов, не содержащих жирных кислот и имеющих особую структуру. К ним относится ряд гормонов, в частности кортизон, вырабатываемый корой надпочечников, различные половые гормоны, регули-рующие белковый, углеводный и минеральный обмен. Холестерин содержится практически во всех тканях организма, входит в состав биологических мембран, укрепляя, стабилизируя их структуру. Нарушение обмена холестерина лежит в основе некоторых патологических состояний. Например, при атеросклерозе он откладывается на стенках кровенос-ных сосудов, что может привести к нарушению кровообращения органов.
• Большое значение имеют гликолипиды (состоят из углеводов и липидов) и липопротеиды (состоят из белков и липи-дов). Особенно их много в составе ткани мозга и нервных волокон.
• Простагландины синтезируются из ненасыщенных жирных кислот. Они регулируют сокращение мускулатуры внут-ренних органов, поддерживают тонус сосудов, регулируют функции различных отделов мозга.
• Листья и плоды многих растений покрыты защитным восковым налетом. Воска вырабатываются и используются в очень больших количествах морскими организмами, особенно планктонными. У позвоночных животных воска секре-тируются кожными железами. Покрывая кожу и ее производные (волосы, шерсть, мех, перья), воска смягчают их и предохраняют от действия воды.

- Фосфолипиды являются основой биологических мембран.
- Как растворители жиры обеспечивают проникновение в организм жирорастворимых веществ, например, витаминов D, Е, А.
Белки: строение и функции.
Белки занимают первое место среди органических веществ, входящих в состав клеток. У животных на них приходится около 50% сухой массы клетки. Их значение и функции в жизнедеятельности чрезвычайно многообразны.
Белки — это биологические непериодические гетерополимеры, мономерами которых являются аминокислоты. Моле-кулы белков представляют собой неветвящиеся структуры (линейные макромолекулы). Аминокислоты чередуются в молекуле полимера нерегулярным образом. Белки представляют собой самый многочисленный и наиболее разнооб-разный класс органических соединений клетки (10 — 20%).
Аминокислоты, входящие в состав полипептидов, имеют как минимум одну аминогруппу (-NH2) и карбоксильную груп-пу (-СООН) и различаются структурой и физико-химическими свойствами радикалов (R). В состав природных белков может входить до 20 разновидностей аминокислот. Восемь аминокислот являются незаменимыми, т.е. клетками чело-века не синтезируются и должны поступать с пищей. Наличие карбоксильной и аминогруппы в составе аминокислот (совмещение свойств кислоты и основания) позволяет им вступать во взаимодействие друг с другом с образованием прочных ковалентных пептидных связей.

Рост полипептидной цепи происходит с N конца в рибосоме. Аминокислоты, соединяясь друг с другом, образуют различной длины пеп-тиды. Пептиды, содержащие от нескольких аминокислотных остатков до нескольких десятков, существуют в организме в свободной фор-ме и обладают высокой биологической активностью. К ним относят ряд гормонов (окситоцин, адренокортикотропный гормон), некоторые очень токсичные ядовитые вещества (например, аманитин грибов), а также многие антибиотики, производимые микроорганизмами.
Число аминокислотных остатков в белковых молекулах варьирует от нескольких сотен до нескольких тысяч. Среди белков организма выделяют простые белки (протеины), состоящие только из аминокислот, и сложные (протеиды), включающие помимо аминокислот так называемые простетические группы различной химической природы (играют важную роль при выполнении белком его биологической функции).
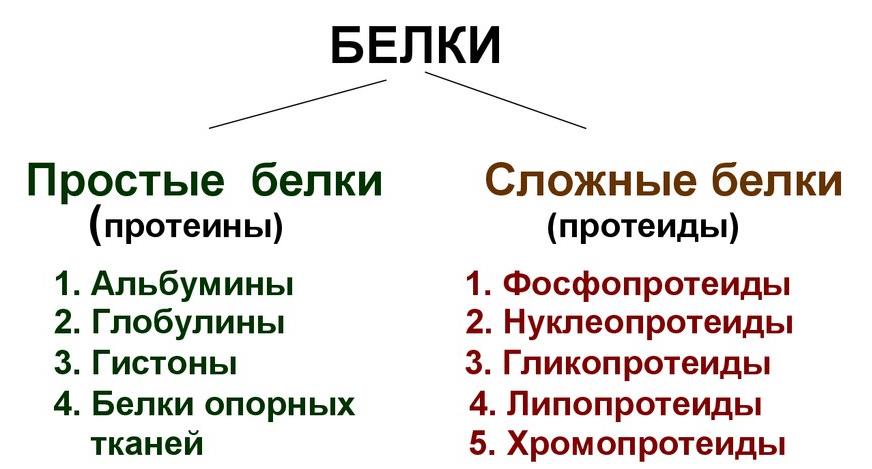
• Липопротеины имеют в своем составе липидный компонент.
• Гликопротеины — углеводный компонент.
• Фосфопротеины имеют одну или несколько фосфатных групп.
• Металлопротеины содержат различные металлы.
• Нуклеопротеины — нуклеиновые кислоты.
Структура белковой молекулы в целом определяется его аминокислотной последова-тельностью, однако она является довольно лабильной и может зависеть от внешних условий, поэтому более правильно говорить о наиболее энергетически выгодной трехмерной структуре (конформации) белка. Различают первичную, вторичную, третичную и четвертичную структуры белковой молекулы.
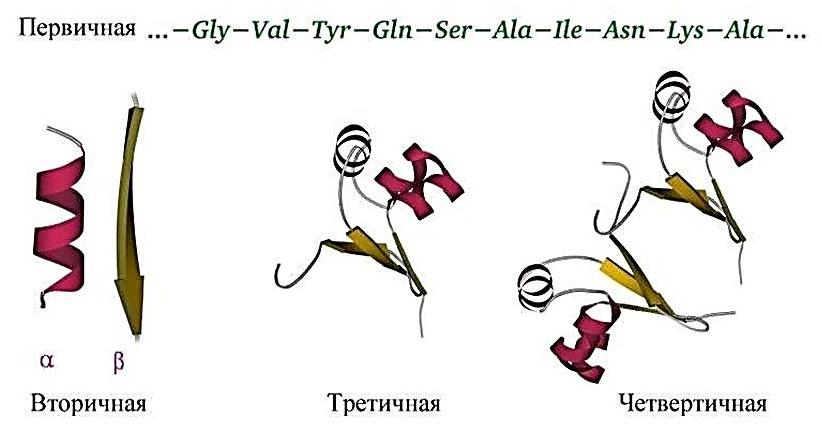
Первичная структура образуется в рибосомах, порядок аминокислот задается в соответствии с генетическим кодом. Она представлена последовательностью аминокис-лотных остатков в составе полипептидной цепи. Белки отличаются друг от друга прежде всего числом, составом и последовательностью аминокислотных остатков. Однако молекула белка в виде цепи аминокислотных остатков (полипептид) еще не способна выполнять специфические функции. Полипептиды в цитоплазме клеток образуют определенную трехмерную простран-ственную конфигурацию (конформация белковой молекулы).
Функциональные свойства белков определяются их конформацией, т.е. расположе-нием полипептидной цепи в пространстве. Уникаль-ность конформации для каждого белка определяется его первичной структурой.
Вторичная структура возникает в результате образования водородных связей между СО- и NH-группами разных аминокислотных остат-ков полипептидной цепи и может иметь вид правильной правозакрученной альфа-спирали (глобин) или складчатой (бета-) структуры (кератин волос).
Третичная структура образуется в результате сложной пространственной укладки молекулы белка. Прочность третичной структуры обес-печивается разнообразными связями, возникающими между радикалами аминокислот (дисульфидными, ионными, гидрофобными). Фор-мирование третичной структуры осуществляется в несколько стадий с участием особых белков, присоединяющих к себе полипептидную цепочку и создающих условия для укладки ее в трехмерную структуру.
Белки могут иметь глобулярную структуру (глобин) или фибриллярную (миозин) структуру. Биологические функции многие белки выполняют на уровне третичной структуры.
Некоторые белки имеют четвертичную структуру, которая представляет собой сложный комплекс, объединяющий несколько третичных структур (например, белок гемоглобин образован четырьмя глобулами), удерживающихся нековалентными ионными, водородными и гидрофобными связями. Гормон поджелудочной железы — инсулин включает две полипептидные цепи. В состав четвертичной структуры некоторых белков помимо белковых субъединиц включаются и разнообразные небелковые компоненты. Например, гемоглобин содержит сложные гетероциклические соединения, содержащие железо.
Белки обладают рядом физико-химических свойств, вытекающих из их структурной организации:
• это преимущественно водорастворимые молекулы, и, следовательно, они могут проявлять свою функциональную активность только в водных растворах;
• белковые молекулы несут поверхностный заряд, влияющий на проницаемость мембран, каталитическую активность;
• белки проявляют свою активность в определенных температурных условиях.
Неблагоприятные условия среды (химические воздействия, высокая температура, облучение, высокое давление и т.д.) вызывают разрушение структуры молекул белков. Нарушение природной структуры белка, а следовательно, свойств и биологической активности назы-вают денатурацией. Денатурация может быть обратимой и необратимой. В первом случае нарушается четвертичная, третичная или вторичная структура и возможен обратный процесс восстановления — ренатурации, во втором — происходит разрыв пептидных связей в составе первичной структуры.
Функции белков чрезвычайно разнообразны. Они основаны на сложности и многообразии форм и состава самих белков.
Ферментная, или каталитическая. Ферменты увеличивают скорость биохимических реакций в десятки и сотни мил-лионов раз. Ферменты высокоспецифичны: каждый фермент катализирует определенный тип реакций, в которых участвуют определенные виды молекул субстратов. Специфичность фермента определяется особенностями структуры его активного центра, строго соответствующего структуре одного или нескольких субстратов. В ходе реакции фермент связывает субстрат, последовательно изменяет его конфигурацию, образуя ряд промежуточных молекул, дающих в конечном итоге продукты реакции. Ускоряющее действие катализаторов в различных реакциях связано с энергией активации — той энергией, которую необходимо сообщить реагирующим молекулам в момент их взаимодействия, чтобы реакция стала возможной. Биологические катализаторы и обеспечивают возможность множеству молекул бес-препятственно вступить во взаимодействия. Активность фермента зависит от ряда факторов: температуры и реакции среды, наличия или отсутствия ряда веществ (например, витаминов, служащих коферментами).

Структурная. Белки являются компонентами клеточных мембран и многих органелл, главным компонентом опорных структур организма (кератин, коллаген).
Сократительная. Тубулины, актины, миозины обеспечивают движение клеток и внутриклеточных структур.
Транспортная заключается в присоединении химических элементов (например, кислорода к гемоглобину) или биологически активных веществ (гормонов) и переносе их к различным тканям и органам тела. Специальные транспортные белки перемещают РНК, синтезированные в клеточном ядре, в цитоплазму. Транспортные белки в составе мембран клеток переносят различные вещества из окружающей среды в цитоплазму, а оттуда — в ядро.
Защитная. Лимфоциты способны синтезировать разнообразные защитные белки — антитела (иммуноглобулины). Их молекулы состоят из четырех полипептидных цепей и имеют участок, узнающий чужеродное вещество и называемый изменчивой областью. Антитела способны распознавать антигены — вещества, несвойственные организму. Антигены могут находиться в крови или в составе вирусов и бактерий. Антитела блокируют антигены, в результате образуется комплекс антиген — антитело, который впоследствии фагоцитируется и разрушается другими формами лейкоцитов. Фибриноген и тромбин защищают организм от кровопотери. Защитную функцию выполняют также антибиотики, синтезируемые некоторыми грибами или бактериями. Эти вещества выделяются в окружающую среду и угнетают процессы жизнедеятельности других организмов — конкурентов. В медицине антибиотики используют для борьбы с инфекционными заболеваниями.
Рецепторная. Молекула рецептора (белок или гликопротеид) специфично реагирует изменением своей пространственной конфигурации на присоединение к ней молекулы определенного химического вещества, передающего внешний регуляторный сигнал, и в свою очередь передает этот сигнал в цитоплазму или ядро. Клетки, принадлежащие к определенному клеточному типу (нервные, мышечные, клетки крови и др.), имеют набор антигенов клеточной поверхности, в состав многих из них входят белки. Такие антигены называют антигенами тканевой принадлежности или тканевой совместимости. Антигены клеточной поверхности демонстрируют принадлежность клетки к тому или иному клеточному типу.
Регуляторная. Специальные белки участвуют в регуляции активности генов, обеспечивая их активацию или репрессию, стимулируют или подавляют клеточное деление, выработку инсулина, гормона роста, соматотропного гормона и др., участвуют в регуляции активности клеток и организма в целом.
Белки, поступающие в составе пищевых продуктов, являются источником аминокислот, высвобождающихся при их расщеплении. Амино-кислоты необходимы в реакциях пластического обмена для построения новых белковых молекул. При полном расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии. Однако белки в таком качестве используются редко.

- Первичная структура белка определяется генотипом.
- Вторичная, третичная и четвертичная структурная организация белков зависит от первичной структуры.
- Все биологические катализаторы — ферменты — имеют белковую природу.
- Белковые молекулы обеспечивают иммунологическую защиту организма от чужеродных веществ.
Вопросы для самопроверки:
- Какие органические вещества входят в состав клетки?
- Из каких малых органических соединений состоят белки?
- Что такое пептиды?
- Что представляет собой первичная структура белка?
- Как образуются вторичная, третичная структуры белка?
- Какой процесс называется денатурацией белка?7. Перечислите и охарактеризуйте функции белков.
Для закрепления пройденного материала перейдите по ссылке: https://learningapps.org/watch?v=poh498znk22
Ферменты.
Большинство ферментов являются белковыми молекулами. Рибозимы (каталитические РНК) также выполняют в клетках некоторые жизненно важные функции, например входят в каталитический центр рибосом (осуществляют биосинтез белка). В отличие от неорганических катализаторов, большинство ферментов обладает высокой специ-фичностью по отношению к своим субстратам и снижают энергию активации реакции очень существенно.
Например: если для реакции разложения пероксида водорода

энергия активации в отсутствие катализатора составляет 75,4 кДж/моль, а при добавлении платины снижается до 42 кДж/моль, то фермент каталаза снижает энергию активации до 2 кДж/моль, что приводит к увеличению скорости ре-акции в сотни тысяч раз.
Классификация ферментов
В 1961 г. в Москве Международный биохимический союз принял современную классификацию ферментов. Все ферменты были разделены на 6 классов по типам катализируемых реакций: класс — оксидоредуктазы; класс — трансферазы; класс — гидролазы; класс — лиазы; класс — изомеразы; класс — лигазы. Внутри каждого класса ферменты сгруппированы по подклассам по природе атакуемой химической группы, а внутри подкласса — на подподклассы по природе акцептора или по характеру атакуемой связи.
Характеристика ферментов различных классов.
Класс I. Оксидоредуктазы
Ферменты данного класса катализируют окислительно-восстановительные реакции, являясь, таким образом, ключевыми в процессах синтеза органических веществ из неорганических и в процессах клеточного дыхания.
Коферментами оксидоредуктаз являются переносчики восстановительных эквивалентов, такие как флавинаденин-динуклеотид (ФАД), флавинмононуклеотид (ФМН), никотинамидадениндинуклеотид (НАД), убихинон, липоевая кислота, гем и другие.
- Дегидрогеназы осуществляют дегидрирование субстрата с использованием любого акцептора водорода, кроме кислорода. Примеры: пируватдегидрогеназа, НАДН-дегидрогеназа.
- Редуктазы являются основными ферментами восстановительных синтезов, например синтеза жирных кислот, синтеза холестерина. Примеры: нитратредуктаза, цитохром P450-редуктаза.
- Оксидазы окисляют субстрат молекулярным кислородом, атомы кислорода не встраиваются в молекулу субстрата. Примеры: пируватоксидаза, НАДФН-оксидаза.
- Монооксигеназы внедряют одну гидроксильную группу в субстраты. Пример: цитохром P450-зависимая монооксигеназа
- Диоксигеназы внедряют два атома кислорода от молекулярного кислорода в молекулу субстрата. Пример: эстрадиол-диоксигеназа.
- Пероксидазы — группа окислительно-восстановительных ферментов, использующих в качестве акцептора электронов пероксид водорода ().
Класс II. Трансферазы
Трансферазы переносят химические группы от одной молекулы к другой. Коферментами трансфераз являются многие водорастворимые витамины и их производные (коэнзим А).
- Киназы переносят фосфатные группы от АТФ на субстрат. Примеры: гексокиназа, фосфофруктокиназа
Класс III. Гидролазы
Гидролазы — ферменты, осуществляющие гидролиз субстрата. Коферменты, как правило, отсутствуют. Рабочие назва-ния гидролаз формируются из названия субстрата с прибавлением окончания «–аза». Примеры: амилаза (расщепляет крахмал), фосфолипаза, экзонуклеаза (расщепляет нуклеиновые кислоты с одного из концов)
Класс IV. Лиазы
Лиазы катализируют разрыв внутримолекулярных связей негидролитическим путём. Коферментами являются тиаминдифосфат, пиридоксальфосфат (производные водорастворимых витаминов), ионы магния и кобальта.
- Декарбоксилазы отщепляют от молекулы субстрата . Пример: пируватдекарбоксилаза
Класс V. Изомеразы
Изомеразы катализируют изомерные превращения в пределах одной молекулы. Коферментами выступают глутатион, производные водорастворимых витаминов (пиридоксальфосфат) и др. Изомеразы подразделяются на следующие группы:
- Рацемазы — участвуют в процессах превращения L- и D-изомеров, R- и S-изомеров. Пример: серин-рацемаза
- Эпимеразы участвуют в процессах превращения изомеров, имеющих более одного асимметричного атома углерода. Пример: рибулозо-5-фосфат-3-эпимераза (рибулоза ксилулоза).
- Мутазы — перенос функциональных групп внутри молекулы. Пример: фосфоглюкомутаза (глюкозо-1-фосфат глюкозо-6-фосфат)
Класс VI. Лигазы
Лигазы катализируют присоединение двух молекул друг к другу с использованием энергии макроэргических связей. Коферменты: нуклеотидтрифосфаты (АТФ), биотин, производные фолиевой кислоты. Тривиальные названия часто образуются из названий получаемого продукта с добавлением основы «–синтетаза», например: глутаминсинтетаза, аминоацил-тРНК-синтетаза и др.
Принцип действия ферментов:
- Фермент взаимодействует с субстратом, но не всей молекулой, а ее отдельным активным центром. При этом образуется фермент-субстратный комплекс.
- Реакция завершается, и этот комплекс распадается, причем достаточно быстро. При этом фермент не меняется и может взаимодействовать с новой молекулой.
Ферменты обладают высокой степенью специфичности действия. Каждый фермент ускоряет только реакции одного типа.
Коферменты.
Коферменты – это такие соединения, которые необходимы, чтобы ферменты могли реализовывать все заложенные природой функции, в том числе каталитические. В природе коферменты витаминов переносят атомы, электроны, некоторые функциональные группы между субстратами. Ферменты – такие белки, которые катализируют химические реакции, свойственные клеткам любой живой ткани. Ферменты и коферменты: одно без другого не существует. Биохимические реакции реализуются с участием многочисленных помощни-ков, в противном случае сложный меха-низм химического взаимодействия живых тканей протекает с нарушениями. Фермент, по своей структуре сложный либо простой белок, нуждается в минералах, коферментах, витаминах. Коферменты – это коэнзим Q10, производные различных витаминов, а также фолиевой кислоты. Коферменты – это огромное разнообразие органических соеди-нений, имеющих относительно сходные функции. Кофермент может стать частью ферментной молекулы в ходе тече-ния химической реакции, при этом претерпевает преобразования, по итогам которых получает свободу. Огромное число коферментов являются производными витаминов. Если в живом организме наблюдаются проблемы с обменом веществ, затрагивающие молекулы витаминов, это зачастую связано с низкой фер-ментной активностью. Особенное внимание в медицине в настоящее время привлекают коферменты, продуцируемые витаминами группы В. Кофермент необходим, чтобы клетка могла продуцировать энергию и выделять ее организму для обеспечения жизне-деятельности. Причем энергия расходуется не только лишь на физическую активность. Внушительных объемов энер-гии требует умственная активность, работа разного рода желез, пищеварительной сис-темы. Довольно затратны на энергию процессы всасывания полезных элементов, поступающих в организм через ЖКТ и другими способами. Сам процесс усвоения также расходует энергетические запасы организма, формируемые благо-даря коферментам и их участию в реакциях с ферментами. Даже кровоток обеспечен именно такими реакциями, без них наша кровь просто не могла бы течь по сосудам! Коэнзим – это такое специфическое вещество, благодаря которому живой организм имеет энергию на реализацию внутренних процессов. Человеческий организм, как удалось подсчитать ученым, содержит порядка сотни триллионов клеток, каждая из которых генерирует энергию для поддержания нормальной жизнедеятельности. При этом клетка не расходует те вещества, которые человек получает вместе с питанием, чтоб восполнить энергетические запасы, но в первую очередь самостоятельно продуцирует энергию. Внешние источники являются запасным вариантом, к которому прибегают в случае недостаточности самостоятельной выработки энергии.
Нуклеиновые кислоты.
Нуклеиновые кислоты — высокомолекулярные органические соединения, обеспечивающие хранение, передачу и реализацию наследственной (генетической) информации в живых организмах. Они были обнаружены в 1869 г. швейцарским химиком Мишнером в ядрах лейкоцитов, чем и обусловлено их название (от лат. nucleus— ядро). Модель строения ДНК предложили Дж. Уотсон и Ф. Крик в 1953 г.
Различают два вида нуклеиновых кислот — дезоксирибонуклеиновые (ДНК) и рибонуклеиновые (РНК). Нуклеиновые кислоты — непериодические линейные гетерополимеры, состоящие из мононуклеотидов.
Каждый нуклеотид состоит из одного пуринового (аденин — А, гуанин — Г) или пиримидинового (цитозин — Ц, тимин — Т, урацил — У) азотистого основания, сахара с пятью углеродными атомами (пентозы — дезоксирибозы или рибозы) и одного-трех остатков фосфорной кислоты.

Каждое пуриновое или пиримидиновое основание связано своим 9-м или 1-м атомом азота с атомом 1-С пентозы, образуя нуклеозид. В молекуле нуклеотида атом 5′-С пентозы нуклеозида связан эфирной связью с фосфатом. В зависимости от числа фосфатных групп различают моно-, ди- и трифосфаты нуклео-тидов, например, аденозинмо-нофосфат — АМФ, гуанозиндифосфат — ГДФ, уридинтрифосфат — УТФ, тимидинтрифосфат — ТТФ и т.д.

Мононуклеотиды самостоятельно принимают участие во множестве биохимических процессах клеток:
- выступают в качестве источников энергии (АТФ, ГТФ);
- используются для внутриклеточного распространения сигналов некоторых биологически активных веществ (цАМФ, цГМФ);
- входят в состав коферментов (ФАД, НАД, НАДФ) и др.;
- рибо- и дезоксирибомононуклеотиды являются предшественниками при биосинтезе полинуклеотидов РНК и ДНК.
Полинуклеотиды ДНК и РНК представляет собой соединенные друг за другом нуклеотиды.
ДНК — дезоксирибонуклеиновая кислота представляет собой генетический материал большинства организмов. В прокариотических клет-ках кроме ДНК в нуклеоиде клетки часто встречаются внехромосомные ДНК — плазмиды. В эукариотических клетках основная масса ДНК находится в клеточном ядре, где она связана с белками в хромосомах ядра, а также содержится в некоторых органоидах — митохондриях и пластидах. ДНК — полимер с очень большой молекулярной массой: в одну молекулу может входить 108 и более нуклеотидов. У нуклеиновых кислот, также, как и у белков можно выделить несколько уровней организации ДНК.
Соединенные друг за другом нуклеотиды образуют полинуклеотидную цепь — первичную структуру ДНК. Нуклеотиды соединяются кова-лентными фосфодиэфирными связями, возникающими между гидроксильной группой у атома 3′-С пентозы одного нуклеотида и фосфат-ной группой у атома 5′-С пентозы следующего нуклеотида. Осевой скелет такой молекулы состоит из чередующихся остатков фосфатов и пентоз, тогда как азотистые основания присоединены сбоку. Такая цепь полярна, она имеет 5′-конец (фосфатный) и 3′-конец (гидрок-сильный).

Полинуклеотидная последовательность цепи ДНК состоит из чередования информатив-ных и неинформативных участков (экзонов и интронов). Последовательность нуклеотидов или азотистых оснований нуклеотидов (первичная структура) ДНК в информатив-ных участках представляет собой материальный эквивалент генетической информации. Каждое сообщение закодировано специфической последовательностью из четырех ос-нований — А, Г, Т и Ц . Функции неинформативных участков ДНК (интронов) точно не установлены. Полагают, что они служат для разделения информативных участков с целью оптимизации процесса генетических рекомбинаций, могут участвовать в структу-рировании хроматина, позволяя участкам генетического материала упаковываться оп-ределенным образом. Другая часть некодирующей ДНК является регуляторной, обеспе-чивающей активность генов.

Вторичная структура ДНК представлена двойной спира-лью, состоящей из двух полинук-леотидных цепей, антипарал-лельно направленных и ориенти-рованных так, что их сахарофос-фатные остовы оказываются снаружи, а азотистые основания — внутри. Основания располагаются парами друг против друга и соединяются водородными связями. Спаривание происходит только между комплементарными (подходящими друг другу) основаниями: одним пуриновым и одним пиримидиновым. Пара А-Т соеди-няется двумя, а Г-Ц — тремя водородными связями. Таким образом, благодаря специфическому спариванию оснований последовательность нуклеотидов в одной цепочке является как бы зеркальным отражением последовательности в другой.
Спираль ДНК характеризуется рядом параметров. Ширина спирали около 2 нм. Шаг, или полный оборот, спирали составляет 3,4 нм и содержит десять пар комплементарных нуклеотидов.

Структуры более высокого порядка образу-ются в результате соединения ДНК с белка-ми. Третичная структура — это супер-спи-раль или кольцо более высокого порядка

Четвертичная структура- объединение нескольких молекул с третичной структурой.
РНК. Рибонуклеиновые кислоты представляют собой полимеры, содержащие от 70 — 80 до нескольких сотен тысяч рибомононуклеотидов, которые соединяются ковалентными 3′-5′-фосфодиэфирными связями, возникающими между гидроксильной группой рибозы одного нуклеотида и фосфатной группой следующего нуклеотида. Образующиеся полинуклеотидные цепи представляют собой сахаро-фосфатный остов, на котором “сидят” четыре вида азотистых оснований. ДНК и РНК как два вида нуклеиновых кислот имеют много общего, но по ряду признаков они отличаются друг от друга.

В РНК углеводным остатком, к которому присоединяются азотистое основание и фосфатная группа, является рибоза, а не дезоксирибоза, как у ДНК. Набор азотистых оснований, входящих в состав РНК, также отличается. Вместо тимина в нуклеотидах РНК стоит другое пиримидиновое основание — урацил. Остальные азотистые основания те же, что и в ДНК — аденин, гуанин и цитозин. В отличие от ДНК молекула РНК состоит только из одной полинуклеотидной цепи. Длина молекулы РНК меньше, чем молекулы ДНК.

РНК представлены разнообразными по размерам, структуре и выполняемым функциям молекулами. Все молекулы РНК являются копиями определенных участков молекул ДНК и синтезируются в ядре. Почти все они непосредственно вовлечены в процесс биосинтеза белка, который в основном осуществляется в цитоплазме эукариотических клеток. Молекулы РНК, выполняющие в цитоплазме функции матриц белкового синтеза, называют матричными, или инфор-мационными, РНК (иРНК). Роль структурных компонентов рибосом выполняют рибосомные РНК (рРНК). Трансляцию (перевод) последовательности азотистых оснований иРНК в последовательность аминокислот в белках обеспечивают адапторные молекулы транспортных РНК (тРНК).

- Нуклеиновые кислоты преимущественно локализованы в клеточном ядре.
- Дезоксирибонуклеиновая кислота — нерегулярный линейный полимер, состоящий из двух полинуклеотидных цепей.
- Наследственная информация заключена в последовательности нуклеотидов ДНК.
- Редупликация ДНК обеспечивает передачу наследственной информации из поколения в поколение.
Вопросы для самопроверки:
- Какие химические элементы входят в состав клетки?
- Что такое микроэлементы и какова их роль в организме?
- Какова роль воды в клетке? Каков характер связи между химическим строением воды и ее ролью в клетке?
- Что такое плазмолиз, тургор, гипертонические, гипотонические, изотонические растворы? Как иначе называются изотонические растворы? Почему?
- На чем основано действие солевого слабительного, гипертонических повязок?
- Какие органические вещества являются источником энергии в клетке?
- В чем заключается значение белков? Какие функции они выполняют в клетке? В организме?
- Что такое ферменты?
- Чем характеризуется строение белков? Что такое первичная, вторичная, третичная структура белка?
- Что такое аминокислоты? Как они соединяются в белковой молекуле?
- Чем определяются многообразие белков и их специфичность?
- Каково биологическое значение углеводов и жиров?
- Что такое мономеры и полимеры? Какие известны биологические полимеры? Как образованы их молекулы?
- Чем отличаются белки от других биополимеров: крахмала, клетчатки?
- Какова роль нуклеиновых кислот в клетке? Какие виды нуклеиновых кислот вы знаете?
- Чем характеризуется строение нуклеотида, ДНК, РНК?
- Что такое “комплементарность” в расположении нуклеотидов ДНК?
- Чем отличается РНК от ДНК?
- Какие разновидности РНК вы знаете? Какова их роль в клетке?
- В чем сходство и различия между белками и нуклеиновыми кислотами?
- Кем и когда предложена модель пространственной организации ДНК?
- Какими параметрами характеризуется двойная спираль ДНК?
- Каковы принципы соединения двух цепей в спирали ДНК?
- Каковы основные функции ДНК как материала наследственности?
АТФ и другие органические вещества клетки.
В любой клетке нашего организма протекают миллионы биохимических реакций. Они катализируются множеством ферментов. Большая часть химических реакций протекает с затратой энергии. Универсальным источником энергии в клетке является АТФ — аденозинтрифосфат, или аденозинтрифосфорная кислота. Вещество является одним из двух наиболее важных источников энергии в любой клетке. Однако АТФ редко непосредственно участвует в реакции: для протекания любого процесса нужна энергия, заключенная в химических связях аденозинтрифосфата (макроэргичес-ких).
Строение молекул АТФ таково, что образующиеся связи между фосфатными группами несут огромное количество энергии. Поэтому такие связи также называются макроэргическими, или макроэнергетическими (макро-много, большое количество). Термин макроэргические связи впервые ввел ученый Ф. Липман, и он же предложил исполь-зовать значок ∞ для их обозначения. Очень важно для клетки поддерживать постоянный уровень содержания аде-нозинтрифосфата. Особенно это характерно для клеток мышечной ткани и нервных волокон, потому что они наибо-лее энергозависимы и для выполнения своих функций нуждаются в высоком содержании аденозинтрифосфата.

Строение молекулы АТФ. Аденозинтрифосфат состоит из трех элементов: рибозы, аденина и остатков фосфорной кислоты. Рибоза – углевод, который относится к группе пентоз. Это значит, что в составе рибозы 5 атомов углерода, которые заключены в цикл. Рибоза соединяется с аденином гликозидной связь на 1-ом атоме углерода. Также к пен-тозе присоединяются ос-татки фосфорной кислоты на 5-ом атоме углерода. Аденин – азотистое основание. В зависи-мости от того, какое азотистое основание присоединяется к рибозе, выделяют также ГТФ (гуанозинтрифосфат), ТТФ (тимидин-трифосфат), ЦТФ (цитидинтрифосфат) и УТФ (уридин-трифосфат). Все эти вещества схожи по строению с аденозинтрифосфатом и выполняют такие же функции, однако они встречаются в клетке намного реже. Остатки фосфорной кисло-ты. К рибозе может присоединиться максимально три остатка фосфорной кислоты. Если их два или только один, то соответственно вещество называется АДФ (дифосфат) или АМФ (монофосфат). Именно между фосфор-ными остатками заключены макроэргические связи, после разрыва которых высвобождается от 40 до 60 кДж энергии. Если разрываются две связи, выделяется 80кДж энергии. При разрыве связи между рибозой и фосфорным остатком выделяется всего лишь 13,8 кДж, поэтому в молекуле трифосфата только две макроэргические связи (Р ̴ Р ̴ Р), а в моле-куле АДФ — одна (Р ̴ Р). По причине того, что между остатками фосфорной кислоты образуется макроэнергетическая связь, строение и функции АТФ связаны между собой. Кроме энергетической, АТФ может выполнять множество других функций в клетке. Наряду с другими нуклеотидтрифосфатами трифосфат участвует в построении нуклеиновых кислот. В этом случае АТФ, ГТФ, ТТФ, ЦТФ и УТФ являются поставщиками азотистых оснований. Это свойство используется в процессах репликации ДНК и транскрипции. Также АТФ необходима для работы ионных каналов. Например, Na-K канал выкачивает 3 молекулы натрия из клетки и вкачивает 2 молекулы калия в клетку. Такой ток ионов нужен для поддержания положительного заряда на наружной поверхности мембраны, и только с помощью аденозинтрифосфата канал может функционировать. То же касается протонных и кальциевых каналов.
Молекулы АТФ быстро используются и разрушаются. Поэтому синтез трифосфата – это важный процесс образования энергии в клетке. Выделяют три наиболее важных способа синтеза аденозинтрифосфата:
1. Субстратное фосфорилирование.
2. Окислительное фосфорилирование.
3. Фотофосфорилирование.
Интересные факты об АТФ — В среднестатистической клетке содержится 0,04% аденозинтрифосфата от всей массы. Однако самое большое значение наблюдается в мышечных клетках: 0,2-0,5%. — В клетке около 1 млрд молекул АТФ. — Каждая молекула живет не больше 1 минуты. — Одна молекула аденозинтрифосфата обновляется в день 2000-3000 раз. — В сумме за сутки организм человека синтезирует 40 кг аденозинтрифосфата, и в каждый момент времени запас АТФ составляет 250 г.

- Вещество играет ключевую роль в процессах жизнедеятельности, ведь в макроэргических связях между фосфатными остатками содержится огромное количество энергии.
- Аденозинтрифосфат выполняет множество функций в клетке, и поэтому важно поддерживать постоянную концентрацию вещества.
- Распад и синтез идут с большой скоростью, т. к. энергия связей постоянно используется в биохимических реакциях.
- Это незаменимое вещество любой клетки организма.
Для закрепления пройденного материала перейдите по ссылке: https://learningapps.org/view27646527
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №1 «Роль белков, углеводов и жиров в организме человека. Витамины.»
ПОДГОТОВЬТЕ СООБЩЕНИЯ по следующим темам.
— изучение роли белков в организме человека;
— изучение роли углеводов в организме человека;
— изучение роли жиров в организме человека;
— изучение роли АТФ в организме человека;
— витамины, гипо- и авитаминозы и их последствия;
— биологически активные добавки, их значение в жизни человека,
ЛАБОРАТОРНАЯ РАБОТА №1 «Определение витамина С в продуктах питания. Гидрофильно-гидрофобные свойства липидов.«
Еще в глубокой древности было известно, что отсутствие некоторых продуктов в пищевом рационе может быть причиной заболеваний.
Отсутствие витаминов в пище может приводить к тяжелым расстройствам в организме. Самым распространенным витамином является витамин С. С давних времен люди страдали от многочисленных тяжелых болезней, причины ко-торых были неизвестны. Одна из таких болезней — цинга, ею обычно болеют люди на Крайнем Севере. Известно, что в экспедиции Васко де Гама от цинги погибло около 60% моряков, такая же судьба постигла русского мореплавателя В. Беринга и многих членов его экипажа в 1741 г., русского полярника Г.Я. Седова в 1914 г. и др. За время существования парусного флота от цинги погибло моряков больше, чем во всех морских сражениях, вместе взятых. И причиной тому был недостаток или гиповитаминоз витамина С.
Витамин С или аскорбиновая кислота представляет собой белые кристаллы, растворимые в воде и имеющие вкус лимонного сока.
История открытия витамина С связана с цингой. В те далекие времена эта болезнь особенно поражала мореплава-телей. Сильные, отважные моряки были бессильны перед цингой, которая к тому же часто вела к смертельному исхо-ду. Болезнь проявлялась общей слабостью, кровоточивостью десен, вследствие чего выпадали зубы, появлялась сыпь, кровоизлияния на коже. Но все же был найден путь излечения. Так, моряки, следуя примеру индейцев, стали пить водный экстракт сосновой хвои, который является кладезем витамина С. В XVIII веке хирург британского флота Дж. Линд показал, что болезнь моряков можно излечить, добавив в их рацион питания свежие овощи и фрукты. Интересен еще другой факт: Альберт фон Сент- Дьердь, первооткрыватель витамина С, на самом деле открыл целый комплекс витаминов.
Огромная заслуга в исследовании его свойств принадлежит Лайнусу Полингу. Лайнус Карл Полинг один из немно-гих ученых, дважды в своей жизни удостаивавшихся высшей мировой оценки заслуг перед человечеством — Нобе-левской премии. Лайнус Полинг — один из основателей современной химии и молекулярной биологии.
БИОЛОГИЧЕСКАЯ ЦЕННОСТЬ ВИТАМИНА С.
Витамин С – мощный антиоксидант. Он играет важную роль в регуляции окислительно-восстановительных про-цессов, участвует в синтезе коллагена и проколлагена, обмене фолиевой кислоты и железа, а также синтезе стероид-ных гормонов и катехоламинов. Аскорбиновая кислота также регулирует свертываемость крови, нормализует прони-цаемость капилляров, необходима для кроветворения, оказывает противовоспалительное и потивоаллергическое действие.
Витамин С является фактором защиты организма oт последствий стресса. Усиливает процессы, увеличивает устой-чивость к инфекциям. Уменьшает эффекты воздействия различных аллергенов. Имеется много теоретических и экс-периментальных предпосылок для применения витамина С с целью профилактики раковых заболеваний. Известно, что у онкологических больных из-за истощения его запасов в тканях нередко развиваются симптомы витаминной недостаточности, что требует дополнительного их введения.
Существуют данные, показывающие профилактическую роль витамина С в отношении рака толстой кишки, пище-вода, мочевого пузыря и эндометрия (Block G., Epidemiology, 1992, 3 (3), 189–191).
Витамин С улучшает способность организма усваивать кальций и железо, выводить токсичные медь, свинец и ртуть.
Важно знать, что в присутствии адекватного количества витамина С значительно увеличивается устойчивость вита-минов В1, В2, A, E, пантотеновой и фолиевой кислот. Витамин С предохраняет холестерин липопротеидов низкой плотности от окисления и, соответственно, стенки сосудов от отложения окисленных форм холестерина.
Наш организм не может запасать витамин С, поэтому необходимо постоянно получать его дополнительно. Поскольку он водорастворим и подвержен действию температуры, приготовление пищи с термической обработкой его разрушает.
СУТОЧНАЯ ПОТРЕБНОСТЬ В ВИТАМИНЕ С.
Суточная потребность человека в витамине С зависит от ряда причин: возраста, пола, выполняемой работы, сос-тояния беременности или кормления грудью, климатических условий, вредных привычек.
Болезни, стрессы, лихорадка и подверженность токсическим воздействиям (таким, как сигаретный дым) увеличивают потребность в витамине С.
В условиях жаркого климата и на Крайнем Севере потребность в витамине С повышается на 30-50 процентов. Моло-дой организм лучше усваивает витамин С, чем пожилой, поэтому у лиц пожилого возраста потребность в витамине С несколько повышается.
Средневзвешенная норма физиологических потребностей составляет 60-100 мг в день. Обычная терапевтическая доза составляет 500-1500 мг ежедневно.

ВИТАМИННАЯ НЕДОСТАТОЧНОСТЬ – АВИТАМИНОЗ.
Недостаточность снабжения организма витаминами ведет к его ослаблению, резкий недостаток витаминов – к на-рушению обмена веществ и заболеваниям – авитаминозам, которые могут окончиться гибелью организма. Авитаминозы могут возникать не только от недостаточного поступления витаминов, но и от нарушения процессов их усваивания и использования в организме.
По данным руководителя лаборатории витаминов и минеральных веществ Института питания РАМН проф.В.Б. Спи- ричева, результаты обследований в разных регионах России, показывают, что подавляющее большинство детей дош-кольного и школьного возраста испытывает недостаток необходимых для их нормального роста и развития витами-нов. Особенно неблагополучно обстоит дело с витамином С, недостаток которого был выявлен у 80–90% обследован-ных детей.
Глубина этого дефицита нарастает в зимне-весенний период, однако у многих детей недостаточная обеспечен-ность витаминами сохраняется даже в более благоприятные летние и осенние месяцы.
Недостаточное потребление витаминов заметно снижает активность иммунной системы, повышает частоту и уси-ливает тяжесть респираторных и желудочно-кишечных заболеваний. Недостаточность может быть экзогенная (за счет недостатка аскорбиновой кислоты в продуктах питания) и эндогенная (за счет нарушения всасываемости и усвояемости витамина С в организме человека).
При недостаточности поступления витамина в течение длительного времени может развиваться гиповитаминоз.
ГИПЕРВИТАМИНОЗ.
Витамин С хорошо переносится даже в высоких дозах. Однако, при слишком больших дозах приема может раз-виться диарея. Большие дозы могут вызвать гемолиз (разрушение красных кровяных клеток) у людей, страдающих отсутствием специфического фермента глюкозо-6-фосфатдегидрогеназы. Поэтому людям с таким нарушением можно принимать повышенные дозы витамина С только под строгим наблюдением врача.
Если аскорбиновую кислоту принимать в больших дозах одновременно с аспирином, может возникнуть раздраже-ние желудка, вследствие чего, разовьется язва (аскорбиновая кислота в виде аскорбата кальция имеет нейтральную реакцию и менее агрессивна по отношению к слизистой желудочно-кишечного тракта). При применении витамина С с аспирином следует также помнить, что большие дозы аспирина могут привести к усиленному выделению витамина С через почки и потере его с мочой и, следовательно, через некоторое время к дефициту витамина. Жевательные конфеты и жевательные резинки с витамином С могут повредить эмаль зубов, следует полоскать рот или чистить зубы после их приема. При беременности не рекомендуется принимать слишком высокие дозы витамина С, поскольку у плода может возникнуть зависимость.
ПРОФИЛАКТИКА АВИТАМИНОЗА.
Комитет экспертов ВОЗ ввел понятие о безусловно допустимой суточной дозе витамина С, которая не превышает 2,5 мг/кг веса тела, и условно допустимой суточной дозе витамина С, которая составляет 7,5 мг/кг (Шилов П.И., Яковлев Т.Н., 1974)
Профилактика витаминной недостаточности заключается в производстве пищевых продуктов, богатых витамина-ми, в достаточном потреблении овощей и фруктов, правильном хранении пищевых продуктов и рациональной тех-нологической обработке их на предприятиях пищевой промышленности, общественного питания и в быту. При не-достатке витаминов — дополнительное обогащение питания витаминными препаратами, витаминизированными пи-щевыми продуктами массового потребления.
Витамин C назначают при цинге, некоторых заболеваниях желудочно-кишечного тракта, кровотечениях, аллергиях, коллагенозах, атеросклерозе, инфекционных заболеваниях, профилактических интоксикациях.
Исследования позволили утверждать, что высокие дозы витамина C способствуют продлению жизни и улучшению состояния больных определенными видами рака. Имеются данные о том, что очень высокие дозы аскорбиновой кис-лоты могут препятствовать нормальному оплодотворению, вызвать выкидыши, повышать свертываемость крови, оказывать неблагоприятное действие на функцию почек и поджелудочной железы. Однако опасность передозировки аскорбиновой кислоты преувеличено. Результаты многочисленных исследований позволили считать, что гипервита-миноз C практически не проявляется.
Систематический прием больших доз витамина C снижает риск возникновения рака полости рта, пищевода, гортани, желудка, молочной железы, мозга. Большие дозы витамина C (около 1 г в сутки) несколько снимают крайне опасное воздействие табачного дыма на организм курильщика.
Помимо витаминных препаратов для профилактики гиповитаминоза используются плоды шиповника. Плоды шиповника отличаются относительно высоким содержанием аскорбиновой кислоты (не менее 0,2%) и широко применяются в качестве источника витамина С. Используют собранные в период созревания и высушенные плоды разных видов кустарников шиповника. Они содержат, помимо витамина С, витамины К, Р, сахара, органические, в том числе дубильные, и другие вещества. Применяют в виде настоя, экстрактов, сиропов, пилюль, конфет, драже.
ИСТОЧНИКИ ВИТАМИНА С.
Первоисточником витаминов служат главным образом растения. В организме человека аскорбиновая кислота не образуется, и отсутствуют ее накопления. Человек и животные получают витамины непосредственно с растительной пищей и косвенно — через продукты животного происхождения. В продуктах животного происхождения витамин С представлен незначительно (печень, надпочечники, почки). Значительное количество аскорбиновой кислоты содер-жится в продуктах растительного происхождения например, цитрусовые, овощи листовые зеленые, дыня, брокколи, брюссельская капуста, цветная и кочанная капуста, черная смородина, болгарский перец, земляника, помидоры, ябло-ки, абрикосы, персики, хурма, облепиха, шиповник, рябина, печеный картофель в «мундире». Травы, богатые витами-ном С: люцерна, коровяк, корень лопуха, песчанка, очанка, семя фенхеля, пажитник сенной, хмель, хвощ, ламинария, мята перечная, крапива, овес, кайенский перец, красный перец, петрушка, сосновые иглы, тысячелистник, подорож-ник, лист малины, красный клевер, плоды шиповника, шлемник, листья фиалки, щавель. Нормы содержания витами-на С в некоторых пищевых продуктах (в мг на 100 г) смотри в приложении 1.
На содержание витамина C в пищевых продуктах значительное влияние оказывает хранение продуктов и их кули-нарная обработка. Витамин C быстро разрушается в очищенных овощах, даже если они погружены в воду. Соление и маринование разрушают витамин C. Кулинарная обработка, как правило, приводит к снижению содержания аскорби-новой кислоты в продукте. Витамин C лучше сохраняется в кислой среде.
Аскорбиновую кислоту можно получать и синтетическим путем, ее выпускают в виде порошка, драже, таблеток с глюкозой и т. д. Аскорбиновая кислота входит в состав различных поливитаминных препаратов.
ПРАКТИЧЕСКАЯ ЧАСТЬ. Количественное определение содержания витамина С в продуктах питания йодометрическим методом
У аскорбиновой кислоты есть свойство, которого нет у всех остальных кислот: быстрая реакция с йодом. Поэтому для ее определения количественного содержания витамина С в продуктах питания используют йодометрический метод..
Одна молекула аскорбиновой кислоты — С6Н8О6 , реагирует с одной молекулой йода – I2.
1. Приготовление рабочих растворов для определения витамина С
Для определения витамина С в соках и других продуктах необходимо взять аптечную йодную настойку с концен-трацией йода 5 %, т.е. 5 г в 100 мл. Однако, аскорбиновой кислоты в некоторых соках может так мало, что на титрова-ние определенного объема сока (например, 20 мл) уходит всего 1-2 капли йодной настойка. При этом ошибка анализа оказывается очень большой. Чтобы результат был точнее, нужно брать много сока, либо разбавить йодную настойку. В обоих случаях число капель йода, израсходованных на титрование, увеличивается, и анализ будет точнее.
Для анализа фруктовых соков удобно к 1 мл йодной настойки добавить прокипяченной воды до общего объема 40 мл, то есть разбавить настойку в 40 раз и 1 мл его соответствует 0,88 мг аскорбиновой кислоты.
Чтобы узнать, сколько будет израсходовано на титрование йодной настойки необходимо вначале определить объём 1 капли: с помощью шприца отмерим 1 мл разбавленного раствора йода и посчитаем, сколько капель из обычной пипетки содержится в этом объеме. В одной капе содержится 0.02 мл.
Далее готовим крахмальный клейстер: для этого вскипятим ½ кружки воды, пока вода нагревается, размешаем 1/4 чайную ложку крахмала с ложкой холодной воды, так чтобы не было комочков. Выльем в кипящую воду и охладим.
2. Испытание растворов на точность.
Прежде чем приступить к анализу продуктов, испытаем наш раствор на точность. Для этого возьмем 1 таблетку чистого витамина, 0.1 г, растворим ее в 0.5 л кипяченой воды. Возьмем для опыта 25 мл, что соответствует содержа-нию витамина в 20 раз меньшей чем в таблетке. Дольем к этому раствору 1/2 чайной ложки крахмального клейстера и по каплям, добавим раствор йода до синего цвета. Определяем число капель и следовательно, объём израсходо-ванного раствора йода, рассчитываем содержание витамина в растворе по формуле: 0.88* V=А мг, где V- объём раствора йода. В исходной таблетке А – в 20 раз больше, то А* 20= содержание аскорбиновой кислоты в таблетке. Результаты показали, что на титрование ушло 6 мл раствора что соответствует 5.28 мг витамина, домножив на 20 находим цифру 105.6 . Это означает что точность нашего анализа вполне достаточна
3. Определение аскорбиновой кислоты в продуктах.
Мы взяли 25 мл исследуемого продукта добавили крахмала. Затем провели титрование раствором йода исследуе-мой жидкости до появления устойчивого синего окрашивания крахмала, которое говорит о том, что вся аскорби-новая кислота окислилась. Записали количество раствора йода, пошедшего на титрование, и произвели расчёт. Для этого мы составили пропорцию, зная что 1 мл 0,125%-ного раствора йода окисляет 0,875 мг аскорбиновой кислоты.
4. Обработка полученных результатов
На титрование 25 мл сока лимона ушло 7.1 мл раствора йода. Составили пропорцию:
1 мл йодного раствора – 0,875 мг аскорбиновой кислоты 7.1 мл – X
X= 7.1 * 0,875/1=6.25 (мг)
Итак, в 25 мл сока содержится 6.25 мг аскорбиновой кислоты. Тогда в 100 мл сока содержится 6.25*100/25=25 мг
Подобным образом мы рассчитали содержание витамина С в остальных продуктах. Полученные данные занесли в таблицу 1.
Таблица 1. Результаты исследований
| Анализируемый продукт | Количество сока для анализа | Объем раствора йода (в мл) | Количество витамина С в 25 мл сока | Количество витамина С в 100мл |
| Сок лимона (свежевыжатый) | 25 | 7,1 | 6,25 | 25 |
| Сок апельсиновый из упаковки | 25 | 4,3 | 3,8 | 15,2 |
| Перец красный сладкий | 25 | 22,7 | 20 | 80 |
| Сок яблока (зимний сорт) | 25 | 0,45 | 0,4 | 1,5 |
| Отвар шиповника | 25 | 109,4 | 96,25 | 385 |
| Аскорбиновая кислота(в таблетках) | 25 | 28,4 | 25 | 100 |
| Капуста белокочанная | 25 | 16 | 14 | 56 |
Таким образом, в ходе выполнения работы, мы пришли к практическому выводу, что витамином С, который необхо-дим для укрепления иммунной системы организма человека, наиболее богатые продукты – отвар шиповника, перец красный, капуста и лимон. Мы бы рекомендовали самое простое – готовить настой из плодов шиповника. Он очень вкусный, особенно с мёдом или фруктовым сиропом, поэтому его с удовольствием можно пить.
Из плодов шиповника можно также готовить сироп, добавляя к ним ягоды красной и черноплодной рябины, калины, клюквы, боярышника. Такой сироп можно употреблять по 1 ст.л. 3 раза в день, а маленьким детям давать 0,5-1 ч.л. – это обеспечит профилактику многих заболеваний.

- Витамины – это важнейший класс незаменимых пищевых веществ. Говоря о витаминах, можно сказать, что важ-ны они все, но витамин С — аскорбиновую кислоту, большинство биохимиков считают одним из величайших чудес живой природы. Молекула аскорбиновой кислоты настолько проста, активна и под-вижна, что она способ-на легко преодолевать множество препятствий, учас-твуя в различных процессах жизнедеятельности.
- Для получения организмом достаточного витамина С необходимо есть либо местные овощи, либо полученную синтетическим путем аскорбиновую кис-лоту.
- Витамин С является одним из самых мощных антиоксидантов, и впервые он был выделен из сока лимона. Он прекрасно растворяется в воде, и это даёт ему ряд преимуществ – например, благодаря этому свойству витамин С может легко и быстро проникать туда, куда нужно, помогать иммунной сис-теме ликвидировать сбои в организ-ме, и запускать процессы, необходимые для здоровья и жизни человека. Однако это же свойство делает его уяз-вимым – аскорбиновая кислота разрушается при тепловой обработке продуктов.
- Исследовать содержание витамина С в пищевых продуктах можно не прибегая к помощи специальной лабора-тории, а сделать это в домашних условиях.
- Витамин С – аскорбиновая кислота, обнаружен во фруктах и овощах при помощи раствора йода.
- Наибольшее количество витамина С содержится в свежих овощах и фруктах, особенно в плодах шиповника, красном перце, лимоне.
Содержание витамина С в некоторых пищевых продуктах (в мг на 100 г)
| Наименование пищевых продуктов | Количество аскорбиновой кислоты | Наименование пищевых продуктов | Количество аскорбиновой кислоты |
| Овощи | Фрукты и ягоды | ||
| Баклажаны | 5 | Абрикосы | 10 |
| Горошек зеленый консервированный | 10 | Апельсины | 50 |
| Горошек зеленый свежий | 25 | Арбуз | 7 |
| Кабачки | 10 | Бананы | 10 |
| Капуста белокочанная | 50 | Брусника | 15 |
| Капуста квашеная | 20 | Виноград | 4 |
| Капуста цветная | 75 | Вишня | 15 |
| Картофель лежалый | 10 | Гранат | 5 |
| Картофель свежесобранный | 25 | Груша | 8 |
| Лук зеленый | 27 | Дыня | 20 |
| Морковь | 8 | Земляника садовая | 60 |
| Огурцы | 10 | Клюква | 15 |
| Перец зеленый сладкий | 125 | Крыжовник | 40 |
| Перец красный | 250 | Лимоны | 50 |
| Редис | 50 | Малина | 25 |
| Редька | 20 | Мандарины | 30 |
| Репа | 20 | Персики | 10 |
| Салат | 15 | Слива | 8 |
| Томатный сок | 15 | Смородина красная | 40 |
| Томат-паста | 25 | Смородина черная | 250 |
| Томаты красные | 35 | Черника | 5 |
| Хрен | 110-200 | Шиповник сушеный | До 1500 |
| Чеснок | Следы | Яблоки, антоновка | 30 |
| Шпинат | 30 | Яблоки северных сортов | 20 |
| Щавель | 60 | Яблоки южных сортов | 5-10 |
| Молочные продукты | |||
| Кумыс | 20 | Молоко кобылье | 25 |
| Молоко козье | 3 | Молоко коровье | 2 |
ПРАКТИЧЕСКАЯ РАБОТА: Изучение свойств липидов и жироподобных веществ: растворимость, эмульгирование, качественная реакция на прогоркшие жиры.
Цель: изучить экспериментальным путём основные физические и химические свойства жиров.
Необходимое оборудование: химические стаканы, пробирки, штативы для пробирок, бюретки, штативы.
Необходимые реактивы: масло подсолнечное нерафинированное, масло сливочное, маргарин, вода, этиловый спирт, бензин, ацетон, бромная вода, раствор яичного белка, раствор мыла, раствор углекислого натрия, диэтиловый эфир, фенолфталеин (спиртовой раствор), раствор КОН (0,1М).
Ход работы:
1. Растворимость липидов.
В четыре пробирки внести по 3 капли нерафинированного растительного масла. После этого в каждую прилить по 2 мл следующих растворов: этиловый спирт, бензин, ацетон, вода. Сравнить результаты. Расположить указанные ве-щества в порядке уменьшения растворимости в них жиров. Выводы оформить в таблице.
2. Определение непредельности высших жирных кислот в жире.
Степень непредельности жиров, обусловленную присутствием непредельных жирных кислот, количественно опре-деляют по присоединению брома или ионов окислителей по месту двойной связи.
В три пробирки поместить соответственно нерафинированное растительное масло (3-4 капли), маргарин и сливочное масло (небольшие порции). После этого в каждую пробирку прилить 10 капель бромной воды. Что наблюдается? На основании наблюдений сделать вывод о количестве непредельных радикалов в различных маслах. Выводы оформить в тетради, подкрепив их уравнением реакции олеиновой кислоты (СН3(СН2)7СН=СН(СН2)7СООН) с бромной водой.
3. Эмульгирование жиров.
Эмульгирование – это процесс дробления крупной капли жира на более мелкие капельки. Известно, что жиры с водой образуют нестойкую эмульсию, которая при стоянии быстро расслаивается из-за слияния капелек масла после взбал-тывания. Добавление специальных веществ – эмульгаторов – снижают поверхностное натяжение и препятствуют слиянию раздробленных частиц жира. К веществам эмульгаторам относятся белок, мыло, щёлочи, соли угольной кислоты и др. В организме основными эмульгаторами жира являются желчные кислоты.
В четыре пробирки прилить соответственно по 2 мл следующих растворов: вода, раствор яичного белка, раствор мы-ла, раствор углекислого натрия. К заданным веществам добавить по 2 капли растительного масла. Пробирки тщатель-но взболтать. С каким из эмульгаторов образовалась наиболее стойкая эмульсия? Расположить эмульгаторы в поряд-ке уменьшения степени эмульгирования в графе «Уравнения и выводы».
4. Качественная реакция на прогоркшие жиры.
Прогорклость жиров обусловлена наличием в них свободных жирных кислот. Чем больше этих кислот, тем сильнее прогорклость. Количество милиграммов КОН, необходимое для нейтрализации кислот, находящихся в 1г жира, назы-вают числом кислотности. Прогорклость жиров происходит под действием света, кислорода и влаги. При этом проис-ходит окисление и гидролиз. Прогорканию способствуют различные микроорганизмы.
10г исследуемого жира поместить в химический стакан и растворить в 30 мл диэтилового эфира. Добавить в раствор 2-3 капли спиртового раствора фенолфталеина. Из бюретки прибавить 0,1-молярный раствор КОН до неисчезающей розовой окраски.
Определить прогорклость жира по следующей системе: в одном миллилитре раствора щёлочи содержится 5,6 мг КОН (по условию). Количественно определённый объём (в мл) раствора гидроксида калия необходимо умножить на 5,6мг. Полученное число разделить на 10. Последнее число будет являться числом кислотности и показывать наличие про-горклости. Если кислотное число выше 6-7, то жир прогорклый.


0 Комментариев