ФЕНОЛЫ.
ФЕНОЛЫ — органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксо-группами.
Оглавление
Классификация фенолов.
Как и спирты, фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп.
Одноатомные фенолы содержат в молекуле одну гидроксильную группу:

Многоатомные фенолы содержат в молекулах более одной гидроксильной группы:
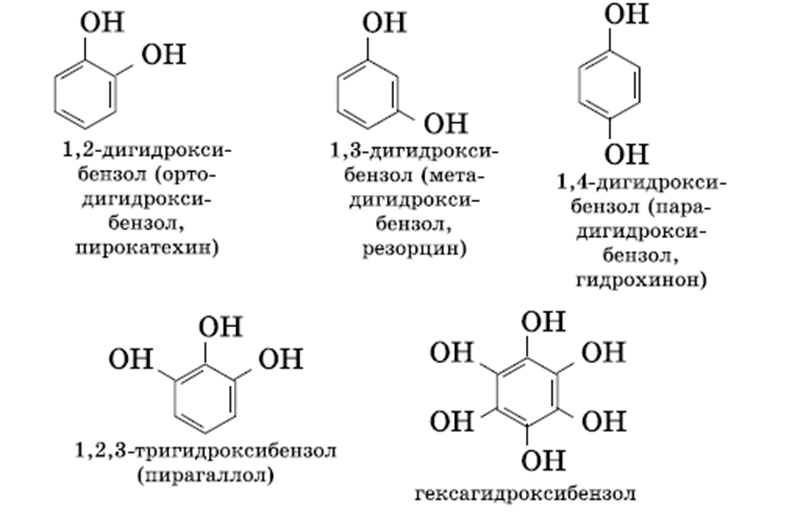
Молекулярная формула фенола С6Н5ОН. Название этого вещества и легло в основу названия всего класса — фенолы.
Физические свойства фенола.
Фенол-твердое, бесцветное кристаллическое вещество с резким характерным запахом, t°плавления=43°С, t°кипения=181°С, ядовитое. Фенол при комнатной температуре незначительно растворяется в воде. Водный раствор фенола называют карболовой кислотой. При попадании на кожу он вызывает ожоги, поэтому с фенолом нужно обращаться очень осторожно!
Строение молекулы фенола.
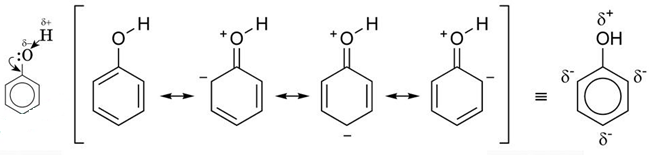
Фенолы в большинстве реакций по связи О–Н активнее спиртов, поскольку эта связь более полярна за счет смещения электронной плотности от атома кислорода в сторону бензольного кольца. Кислотность фенолов значительно выше, чем спиртов.

Для фенолов реакции по месту разрыва связи С-О не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения. Взаимное влияние атомов в молекуле фенола проявляется не только в особен-ностях поведения гидроксогруппы, но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара-положениях (+М-эффект ОН-группы).
Однако кислотные свойства у фенола выражены слабее, чем у неорганических и карбоновых кислот. Кислотные свойства фенола примерно в 3000 раз меньше, чем у угольной кислоты. Поэтому, пропуская через водный раствор фенолята натрия углекислый газ, можно выделить свободный фенол.

Добавление к водному раствору фенолята натрия соляной или серной кислоты также приводит к образованию фенола:
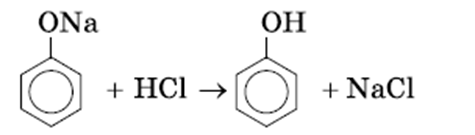
Получение фенола.
Щелочной гидролиз галогенпроизводных аренов:

Кумольный способ:
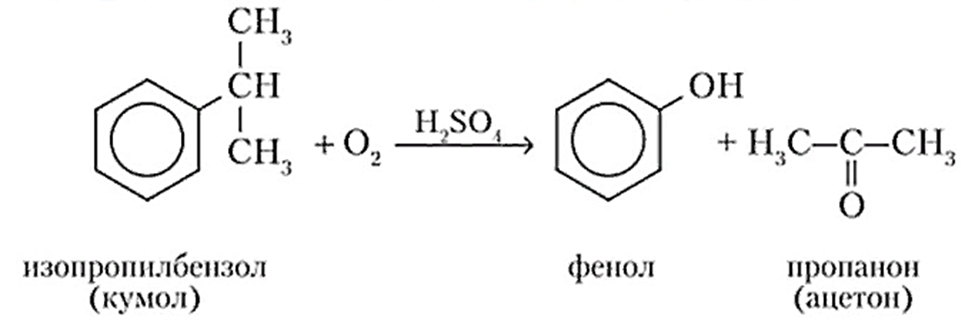
Щелочное плавление солей ароматических сульфоновых кислот:


Для лучшего усвоения данного материала посмотрите видео-урок «Фенолы», перейдя по ссылке:https://youtu.be/edDJjTnPv_Y
Химические свойства фенола.
Кислотные свойства фенола (реакции, идущие по гидроксильной группе). — взаимодействие со щелочными и щелочно-земельными металлами:

-взаимодействие со щелочами:
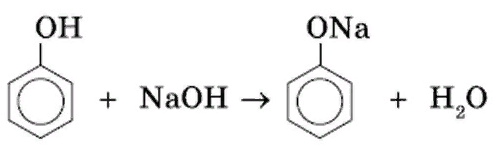
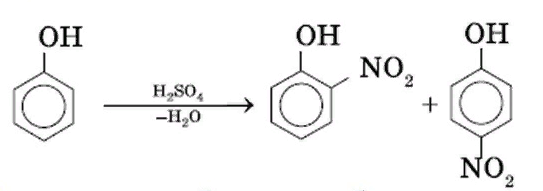
Реакции замещения (по бензольному кольцу) -взаимодействие с азотной кислотой (реакция нитрования):
При недостатке азотной кислоты, в присутствии конц. серной кислоты образуется смесь продуктов: орто-нитрофенол и пара-нитрофенол.
А при взаимодействии фенола с избытком азотной кислоты замещение атомов водорода бензольного кольца происходит в поло-жении 2, 4 и 6, образуется 2,4,6- тринитритфенол (пикриновая кислота), взрывчатое вещество.

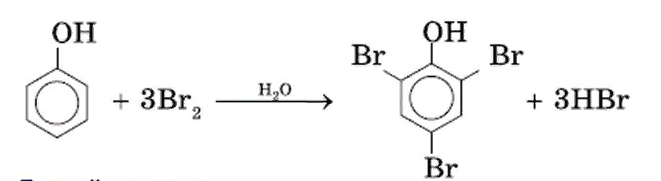
-взаимодействие с галогенами (бромирование).
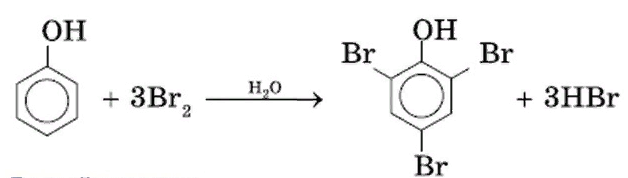
-гидрирование фенола в присутствии катализатора:

Реакция поликонденсации.

Образование линейных молекул происходит при обычной температуре. Проведение этой же реакции при нагревании приводит к тому, что образующийся продукт имеет разветвленное строение, он твердый и нерастворим в воде.
Качественные реакции на фенол.
Взаимодействие с хлоридом железом (III):
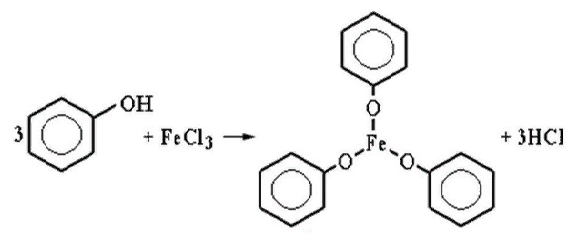
Взаимодействие с бромной водой (обесцвечивание бромной воды) с выпадением осадка белого цвета:

Для лучшего усвоения данного материала посмотрите видео-урок «Фенолы. Химические свойства», перейдя по ссылке:https://youtu.be/OFwQjZ8fTNk
Применение фенола и его соединений.
Фенол — твердое вещество, с характерным запахом, вызывает ожоги при попадании на кожу. Ядовит. Растворяется в воде, его раствор называют карболовой кислотой (антисептик). Она была первым антисептиком введенным в хирургию. Широко использует- ся для производства пластмасс, лекарственных средств (салициловая кислота и ее производные), красителей, взрывчатых веществ. В результате нагревания фенолформальдегидной смолы линейного строения с избытком альдегида получаются твердые пласти- ческие массы с уникальными свой-ствами. Полимеры на основе фенолформальдегидных смол применяют для изготовления лаков и красок, пластмассовых изделий, устойчивых к нагреванию, охлаждению, действию воды, щелочей, кислот. Они обладают высокими диэлектрическими свойствами. Из полимеров на основе фенолформальдегидных смол изготавливают наиболее ответственные и важные детали электроприборов, корпуса силовых агрегатов и детали машин, полимерную основу печатных плат для радиопри-боров. Клеи на основе фенолформаль-дегидных смол способны надежно соединять детали самой различной природы, сохраняя высочайшую прочность соединения в очень широком диапазоне температур. Такой клей применяется для крепления металличес-кого цоколя ламп освещения к стеклян-ной колбе. Таким образом, фенол и продукты на его основе находят широкое применение.
Для закрепления материала по теме «Спирты. Фенолы», перейдите по ссылке: https://learningapps.org/watch?v=p99b3247j23 и выполните задания.


0 Комментариев