КАРБОНОВЫЕ КИСЛОТЫ.
Карбоновые кислоты – это кислородсодержащие органически вещества, молекулы которых содержат одну или несколько карбоксильных групп (-СOOH), соединённых с углеродным радикалом или водородным атомом.
Карбоксильная группа содержит две функциональные группы – карбонил >С=О и гидроксил -OH, непосредственно связанные друг с другом:

Классификация.
А) По числу карбоксильных групп в молекуле:

Б) По природе углеводородного радикала:

Изомерия.
I. Структурная
А) Изомерия углеродного скелета (начиная с C4)
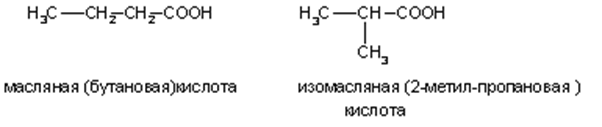
Б) Межклассовая со сложными эфирами R- CO – O- R1 (начиная с C2); Например: для С3Н6О2 — CH3-CH2-COOH пропионовая кислота и СH3-CO-OCH3 метиловый эфир уксусной кислоты.
II. Пространственная
А) Оптическая
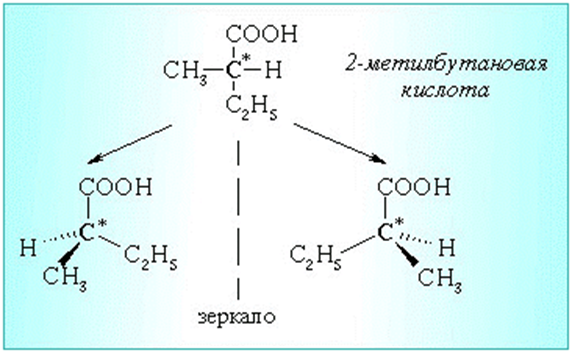
Б) Цис- транс – изомерия для непредельных кислот
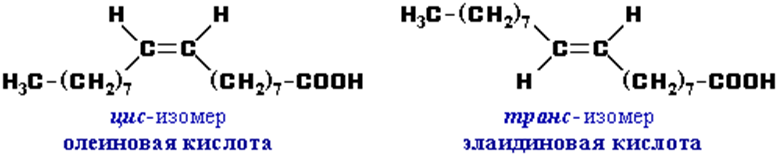
Номенклатура карбоновых кислот.
Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота.
Чтобы указать положение заместителя (или радикала), нумерацию углеродной цепи начинают от атома углерода карбоксильной группы. Например, соединение с разветвленной углеродной цепью (CH3)2CH-CH2-COOH называется 3-метилбутановая кислота. Для органических кислот широко используются также тривиальные названия, которые обычно отражают природный источник, где были впервые обнаружены эти соединения.
| Формула | Название кислоты R-COOH | Название остатка RCOO— | |
| систематическое | тривиальное | ||
| HCOOH | метановая | муравьиная | формиат |
| CH3COOH | этановая | уксусная | ацетат |
| C2H5COOH | пропановая | пропионовая | пропионат |
| C3H7COOH | бутановая | масляная | бутират |
| C4H9COOH | пентановая | валерьяновая | валерат |
| C5H11COOH | гексановая | капроновая | капрат |
| C15H31COOH | гексадекановая | пальмитиновая | пальмитат |
| C17H35COOH | октадекановая | стеариновая | стеарат |
| C6H5COOH | бензолкарбоновая | бензойная | бензоат |
| CH2=СH-COOH | пропеновая | акриловая | акрилат |
Для многоосновных кислот применяют суффиксы -диовая, -триовая и т.д. Например: HOOC-COOH — этандиовая (щавелевая) кислота; HOOC-CH2-COOH — пропандиовая (малоновая) кислота.
ПРЕДЕЛЬНЫЕ ОДНООСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ.
CnH2n+1-COOH или CnH2nO2
Гомологический ряд.
| Название кислоты | Формула кислоты | tпл. °C | tкип. °C | ρ г/см3 | |
| муравьиная | метановая | HCOOH | 8,3 | 100,5 | 1,22 |
| уксусная | этановая | CH3COOH | 16,8 | 118 | 1,05 |
| пропионовая | пропановая | CH3CH2COOH | -21 | 141 | 0,99 |
| масляная | бутановая | CH3(CH2)2COOH | -6 | 164 | 0,96 |
Строение карбоксильной группы.
Карбоксильная группа сочетает в себе две функциональные группы – карбонил >C=O и гидроксил -OH, взаимно влияющие друг на друга:
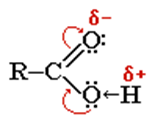
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О–Н. В водном растворе карбоновые кислоты диссоциируют на ионы:
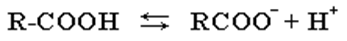
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей.
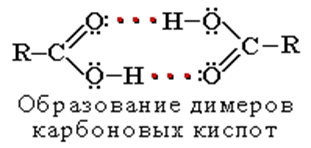
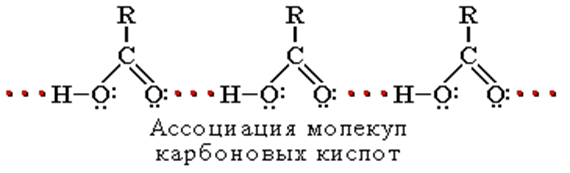
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
Физические свойства предельных одноосновных кислот.
Низшие члены этого ряда при обычных условиях представляют собой жидкости, обладающие характерным острым запахом: этано-вая (уксусная) кислота имеет характерный «уксусный» запах. Безводная уксусная кислота при комнатной температуре представляет собой жидкость; при 17 °С она замерзает, превращаясь в льдистое вещество, которое получило название «ледяная» уксусная кислота. Средние представители этого гомологического ряда — вязкие, «маслообразные» жидкости; начиная с С10 — твердые вещества.
Простейший представитель – муравьиная кислота НСООН – бесцветная жидкость с т. кип. 101 °С, а чистая безводная уксусная кислота CH3COOH при охлаждении до 16,8 °С превращается в прозрачные кристаллы, напоминающие лед (отсюда ее название ледяная кислота).

Для усвоения изученного материала посмотрите видео-урок, перейдя по ссылке: https://youtu.be/pJ1uH94VUoU
Химические свойства карбоновых кислот.
Карбоновые кислоты проявляют высокую реакционную способность. Они вступают в реакции с различными веществами и образуют разнообразные соединения, среди которых большое значение имеют функциональные производные, т.е. соединения, полученные в результате реакций по карбоксильной группе.
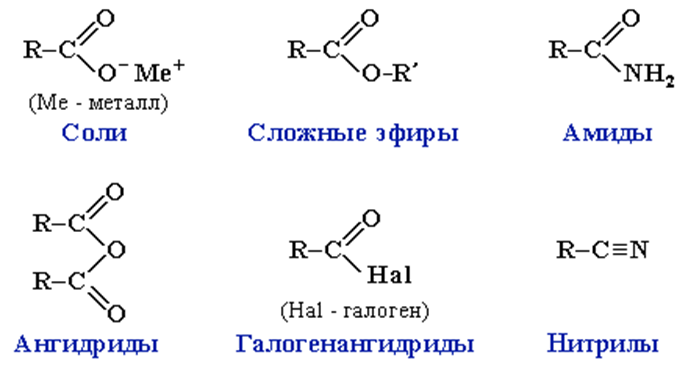
Названия солей составляют из названий остатка RCOO– (карбоксилат-иона) и металла. Например, CH3COONa – ацетат натрия, (HCOO)2Ca – формиат кальция, C17H35COOK – стеарат калия и т.п.
Карбоновые кислоты проявляют химические свойства характерные для неорганических кислот.
1. Диссоциация: R-COOH ↔ RCOO— + H+
-Сила кислот уменьшается в ряду: H-COOH > CH3-COOH > CH3-CH2-COOH
2. Взаимодействие с активными металлами: 2R-COOH + 2Na → 2R-COONa + H2↑
3. Взаимодействие с основными оксидами и основаниями: 2R-COOH + CaO → (R-COO)2Ca + H2O R-COOH + NaOH → R-COONa + H2O
4. Взаимодействие с солями слабых кислот: R-COOH + NaHCO3 → R-COONa + H2O + CO2↑
Соли карбоновых кислот разлагаются сильными минеральными кислотами: R-COONa + HСl → NaCl + R-COOH
-В водных растворах гидролизуются: R-COONa + H2O ↔ R-COOH + NaOH
5. Образование сложных эфиров со спиртами:

Для карбоновых кислот характерны специфические химические свойства
1. Образование функциональных производных R-CO-X (реакции по гидроксильной группе)
Получение хлорангидридов: R-COOH + PCl5 → R-CO-Cl + POCl3 + HCl
2. Образование амидов: CH3COOH + NH3→CH3COONH4 t˚C→ CH3CONH2 + H2O
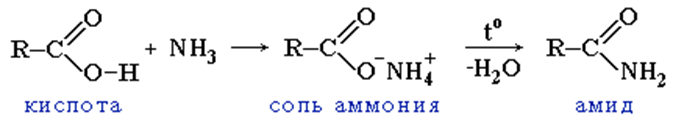
Вместо карбоновых кислот чаще используют их галогенангидриды:
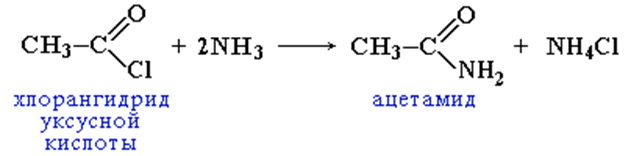
Амиды образуются также при взаимодействии карбоновых кислот (их галогенангидридов или ангидридов) с органическими производными аммиака (аминами):
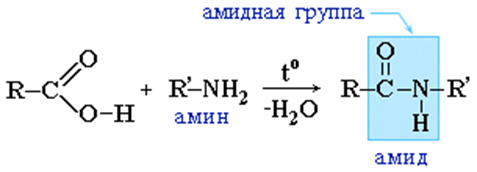
Амиды играют важную роль в природе. Молекулы природных пептидов и белков построены из a-аминокислот с участием амидных групп — пептидных связей.
3. Реакции замещения с галогенами (реакции по углеводородному радикалу с образованием а-хлорпроизводных карбоновых кислот):

4. Особенности муравьиной кислоты H-COOH: Даёт реакцию «Серебряного зеркала»:
H-COOH + 2[Ag(NH3)2]OH → 2Ag↓ + (NH4)2CO3 + 2NH3 + H2O
Окисление хлором: H-COOH + Cl2 → CO2 + 2HCl
Вступает в реакцию с гидроксидом меди(II): H-COOH + 2Cu(OH)2 t → Cu2O↓ + CO2↑ + 3H2O
Разлагается при нагревании: HCOOH t,H2SO4→ CO↑ + H2O
5. Реакции декарбоксилирования солей карбоновых кислот (получение алканов): R-COONa + NaOH t → Na2CO3 + R-H (алкан) 6. Окисление в атмосфере кислорода: R-COOH + O2 → CO2 + H2O

Для усвоения изученного материала посмотрите видео-урок, перейдя по ссылке: https://youtu.be/X1jrIBMeoUo
Получение карбоновых кислот.
I. В промышленности
1. Выделяют из природных продуктов (жиров, восков, эфирных и растительных масел).
2. Окисление алканов:
2CH4 + + 3O2 t,kat → 2HCOOH + 2H2O метан муравьиная кислота
2CH3-CH2-CH2-CH3 + 5O2 t,kat,p → 4CH3COOH + 2H2O н-бутан уксусная кислота
3. Окисление алкенов:
CH2=CH2 + O2 t,kat → CH3COOH этилен
СH3-CH=CH2 + 4[O] t,kat → CH3COOH + HCOOH (уксусная кислота+муравьиная кислота)
4. Окисление гомологов бензола (получение бензойной кислоты): C6H5-CnH2n+1 + 3n[O] KMnO4,H+→ C6H5-COOH + (n-1)CO2 + nH2O 5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5-COOH + 3K2SO4 + 6MnSO4 + 14H2O толуол бензойная кислота
5. Получение муравьиной кислоты:
1 стадия: CO + NaOH t,p → HCOONa (формиат натрия – соль)
2 стадия: HCOONa + H2SO4 → HCOOH + NaHSO4
6. Получение уксусной кислоты: СH3OH + CO t,p → CH3COOH
II. В лаборатории
1. Гидролиз сложных эфиров:

2. Из солей карбоновых кислот:
R-COONa + HCl → R-COOH + NaCl
3. Растворением ангидридов карбоновых кислот в воде: (R-CO)2O + H2O → 2 R-COOH
4. Щелочной гидролиз галоген производных карбоновых кислот:
III. Общие способы получения карбоновых кислот
1. Окисление альдегидов: R-COH + [O] → R-COOH
Например, реакция «Серебряного зеркала» или окисление гидроксидом меди (II) – качественные реакции альдегидов
2. Окисление спиртов: R-CH2-OH + 2[O] t,kat → R-COOH + H2O
3. Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода.

4. Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь: СH3-Br + Na-C≡N → CH3-CN + NaBr
СH3-CN + 2H2O t → CH3COONH4 метилцианид ( нитрил уксусной кислоты) ацетат аммония
CH3COONH4 + HCl → CH3COOH + NH4Cl
5. Использование реактива Гриньяра: R-MgBr + CO2 → R-COO-MgBr H2O → R-COOH + Mg(OH)Br

Для усвоения изученного материала посмотрите видео-урок, перейдя по ссылке: https://youtu.be/xk1yagmBMlo
Применение карбоновых кислот.
Муравьиная кислота – в медицине — муравьиный спирт (1,25% спиртовой раствор муравьиной кислоты), в пчеловодстве, в органи-ческом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя. Впервые была выделена в XVII веке из красных лесных муравьев. Содержится также в соке жгучей крапивы. Безводная муравьиная кислота – бесцветная жидкость с острым запахом и жгучим вкусом, вызывающая ожоги на коже. Применяется в текстильной промышленности в качестве протравы при крашении тканей, для дубления кож, а также для различных синтезов.
Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество. Широко распространена в природе – содержится в выделениях животных (моче, желчи, испражнениях), в растениях (в зеленых листьях). Образуется при брожении, гниении, скисании вина, пива, содержится в кислом молоке и сыре. Температура плавления безводной уксусной кислоты + 16,5°C, кристаллы ее прозрачны как лед, поэтому ее называют ледяной уксусной кислотой. Впервые получена в конце XVIII века русским ученым Т. Е. Ловицем. Натуральный уксус содержит около 5% уксусной кислоты. Из него приготовляют уксусную эссенцию, используемую в пищевой промышленности для консервирования овощей, грибов, рыбы. Уксусная кислота широко используется в химической промышленности для различных синтезов.
Масляная кислота – для получения ароматизирующих добавок, пластификаторов и флотореагентов.
Щавелевая кислота – в металлургической промышленности (удаление окалины).
Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH – в качестве поверхностно-активных веществ, смазочных мате-риалов в металлообработке.
Олеиновая кислота C17H33COOH – флотореагент и собиратель при обогащении руд цветных металлов.

Представители ароматических и непредельных карбоновых кислот
Бензойная кислота C6H5COOH — наиболее важный представитель ароматических кислот. Распространена в природе в растительном мире: в бальзамах, ладане, эфирных маслах. В животных организмах она содержится в продуктах распада белковых веществ. Это кристаллическое вещество, температура плавления 122°C, легко возгоняется. В холодной воде растворяется плохо. Хорошо растворяется в спирте и эфире.
Ненасыщенные непредельные кислоты с одной двойной связью в молекуле имеют общую формулу CnH2n-1COOH.
Высокомолекулярные непредельные кислоты часто упоминаются диетологами (они называют их ненасыщенными). Самая распро-страненная из них – олеиновая СН3–(СН2)7–СН=СН–(СН2)7–СООН или C17H33COOH. Она представляет собой бесцветную жидкость, затвердевающую на холоде.
Особенно важны полиненасыщенные кислоты с несколькими двойными связями:линолевая СН3–(СН2)4–(СН=СН–СН2)2–(СН2)6–СООН или C17H31COOH с двумя двойными связями, линоленовая СН3–СН2–(СН=СН–СН2)3–(СН2)6–СООН илиC17H29COOH с тремя двойными связями и арахидоновая СН3–(СН2)4–(СН=СН–СН2)4–(СН2)2–СООН с четырьмя двойными связями; их часто называют незаменимыми жирными кислотами. Именно эти кислоты обладают наибольшей биологической активностью: они участвуют в переносе и обмене холестерина, синтезе простагландинов и других жизненно важных веществ, поддерживают структуру клеточных мембран, необхо-димы для работы зрительного аппарата и нервной системы, влияют на иммунитет. Отсутствие в пище этих кислот тормозит рост животных, угнетает их репродуктивную функцию, вызывает различные заболевания. Линолевую и линоленовую кислоты организм человека сам синтезировать не может и должен получать их готовыми с пищей (как витамины). Для синтеза же арахидоновой кис-лоты в организме необходима линолевая кислота. Полиненасыщенные жирные кислоты с 18 атомами углерода в виде эфиров гли-церина находятся в так называемых высыхающих маслах–льняном, конопляном, маковом и др. Линолевая кислота C17H31COOH и линоленовая кислота C17H29COOH входят в состав растительных масел. Например, льняное масло содержит около 25% линолевой кислоты и до 58% линоленовой.
Сорбиновая (2,4-гексадиеновая) кислота СН3–СН=СН–СН=СНСООН была получена из ягод рябины (на латыни – sorbus). Эта кислота – прекрасный консервант, поэтому ягоды рябины не плесневеют.
Простейшая непредельная кислота, акриловая СН2=СНСООН, имеет острый запах (на латыни acris – острый, едкий). Акрилаты (эфиры акриловой кислоты) используются для получения органического стекла, а ее нитрил (акрилонитрил) – для изготовления синтетичес-ких волокон.
Называя вновь выделенные кислоты, химики дают волю фантазии. Например: название ближайшего гомолога акриловой кисло-ты, кротоновой СН3–СН=СН–СООН, происходит вовсе не от крота, а от растения Croton tiglium, из масла которого она была выделена. Очень важен синтетический изомер кротоновой кислоты –метакриловая кислота СН2=С(СН3)–СООН, из эфира которой (метилмета-крилата), как и из метилакрилата, делают прозрачную пластмассу – оргстекло.
Непредельные карбоновые кислоты способны к реакциям присоединения:
СН2=СН-СООН + Н2 → СН3-СН2-СООН
СН2=СН-СООН + Сl2 → СН2Сl-СНСl-СООН
СН2=СН-СООН + HCl → СН2Сl-СН2-СООН
СН2=СН-СООН + Н2O → НО-СН2-СН2-СООН
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации.
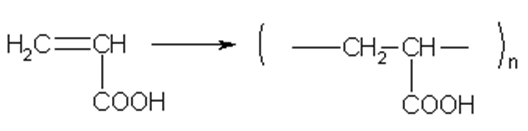
Для лучшего закрепления изученного материала перейдите по ссылке: https://learningapps.org/watch?v=pyr2y0eta23 и выполните задания.


0 Комментариев